Jaana Rautava, Maria Bankvall, Cecilie Gudveig Gjerde, Mats Jontell, Erik Dabelsteen, Palle Holmstrup og Tine M. Søland
Differentialdiagnostik af mundslimhindesygdomme
Associate professor, ph.d., HUS Head and Neck Center, Department of Oral and Maxillofacial Diseases, University Hospital Area, University of Helsinki, Finland
Tandlæge, ph.d., Department of Dental Medicine, Karolinska Institutet, Stockholm/Masthuggskliniken – Orofacialmedicinskt Centrum i Västra Götaland, Göteborg, Sweden
Førsteamanuensis, ph.d. Avdeling for oral og maxillofacial kirurgi, Institutt for klinisk odontologi, Universitetet i Bergen, Norge
Professor emeritus, odont.dr., Department of Oral Medicine and Pathology, Institute of Odontology, Sahlgrenska Academy, University of Gothenburg, Sweden
Professor emeritus, dr.odont., Odontologisk Institut, Det Sundhedsvidenskabelige Fakultet, Københavns Universitet, Danmark
Professor emeritus, dr.odont., ph.d., Odontologisk Institut, Det Sundhedsvidenskabelige Fakultet, Københavns Universitet, Danmark
Førsteamanuensis, ph.d., Institutt for oral biologi, Universitetet i Oslo, Norge
Klinisk relevans
En forudsætning for korrekt behandling af mundslimhindesygdomme er, at man når frem til en korrekt diagnose. Denne korte artikels formål er at give klinikerne redskaber til at skelne mellem forskellige mundslimhindelidelser, der klinisk fremtræder ens.
Det er en indlysende forudsætning for håndtering og behandling af mundslimhindesygdomme, at man når frem til en korrekt diagnose. Imidlertid er der ikke så mange tilfælde af mundslimhindelidelser i almen praksis, at det er muligt at opnå tilstrækkelig rutine. Derfor kan det være vanskeligt at diagnosticere disse tilstande, og formålet med denne artikel er i kort form at give klinikerne relevante værktøjer til at skelne mellem forskellige tilstande med lignende kliniske udseende, fx ulcerøse/vesikulære/bulløse læsioner, farveforandringer, herunder hvide, erytematøse og pigmenterede læsioner samt læsioner med tilvækst af væv.
Artiklens omfang tillader ikke en fremstilling af alle mundslimhindelidelser, og vi har derfor begrænset os til nogle af de i den foregående artikel omtalte, som er de mest relevante i daglig praksis.
Ulcerøse og vesikulære/bulløse læsioner
Recidiverende herpes labialis og læbecancer
Herpes labialis giver sjældent anledning til differentialdiagnostiske problemer, da tilstanden afficerer det samme område og viser sig som initiale vesikler, der brister, flyder sammen og efterlader et sår med skorpe (Fig. 1A). I modsætning til læbecancer (figur 1B) er herpes labialis recidiverende og heler i løbet af 10-14 dage, hvilket er en markant klinisk forskel [1].
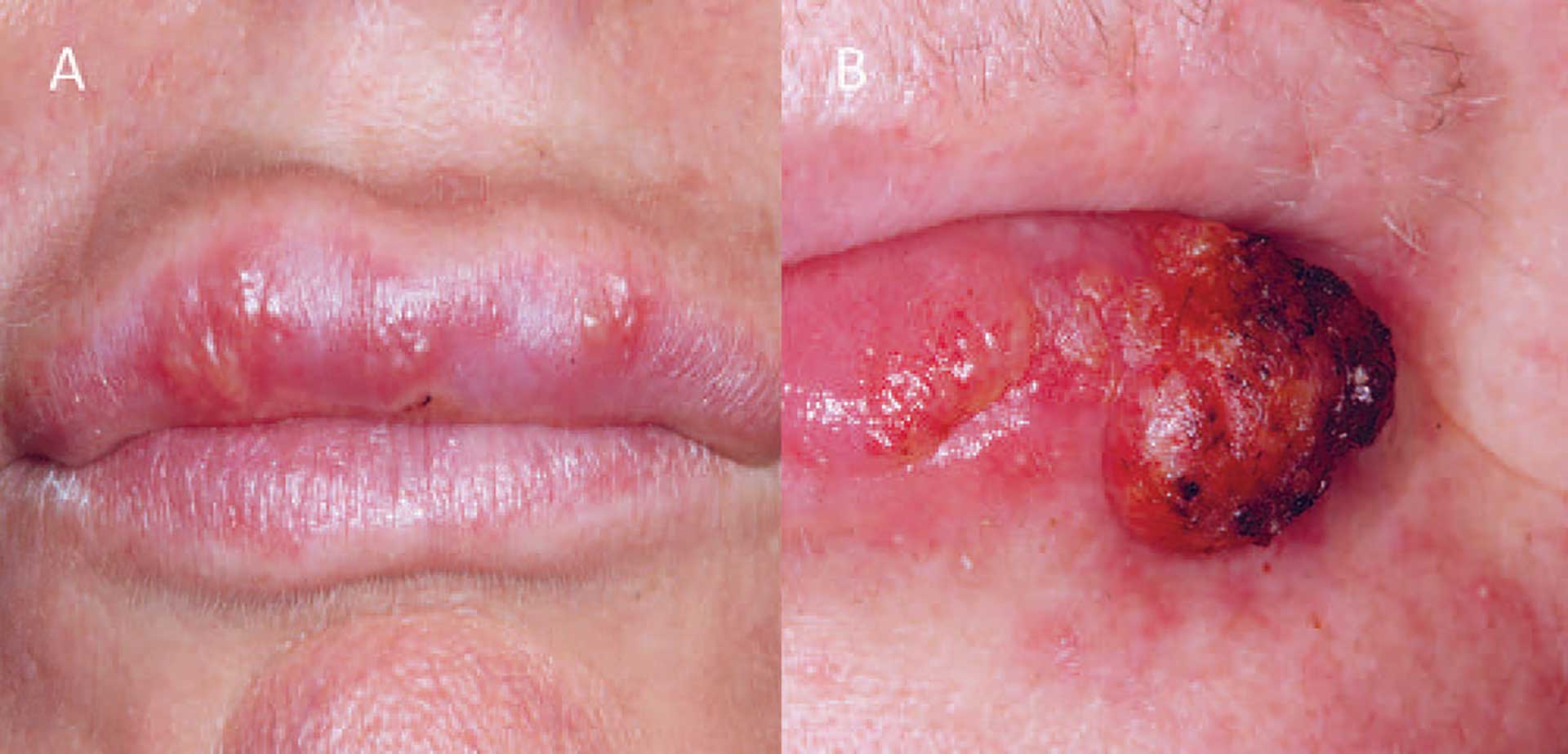
Fig. 1. A. Herpes labialis. B. Læbecancer.
Aftøs stomatitis og virusinfektioner
Flere ulcerøse lidelser manifesterer sig i begyndelsen som vesikler, der måske ikke bliver erkendt, fordi de hurtigt brister og efterlader sår, som sædvanligvis er de læsioner, der bliver diagnosticeret. De mest almindelige ulcerøse læsioner i mundslimhinden er recidiverende aftøs stomatitis/aftelignende ulcerationer. Disse tilstande præsenterer sig som solitære eller multiple smertende, fibrindækkede, cirkulære ulcerationer af varierende størrelse (diameter fra 1 mm til mere end 10 mm), typisk omgivet af en rød halo (figur 2A). Flere tætsiddende ulcerationer kan flyde sammen til atypiske uregelmæssige læsioner. Aftøse ulcerationer kan afficere alle ikke-keratiniserede områder af mundslimhinden og heler sædvanligvis i løbet af 7–10 dage. Større læsioner, som er dybere og mere smertevoldende kan dog persistere i flere uger og eventuelt hele med ardannelse [2] (figur 2B). De aftøse læsioners recidiverende natur adskiller dem fra andre ulcerøse lidelser.
Ved primær herpetisk gingivostomatitis forårsaget af herpes simplex virus 1 eller 2 ses multiple vesikler i mundslimhinden, og tilstanden er ofte ledsaget af feber, især hvis den debuterer i ung alder (figur 2C). Sygdommen viser lokale eller vidt udbredte vesikler, som brister og efterlader cirkulære ulcerationer, der ofte flyder sammen til uregelmæssige fibrindækkede læsioner (figur 2D) [1]. I modsætning til aftøs stomatitis kan denne infektion ramme alle dele af mundslimhinden, og den ses ofte på gingiva [2].
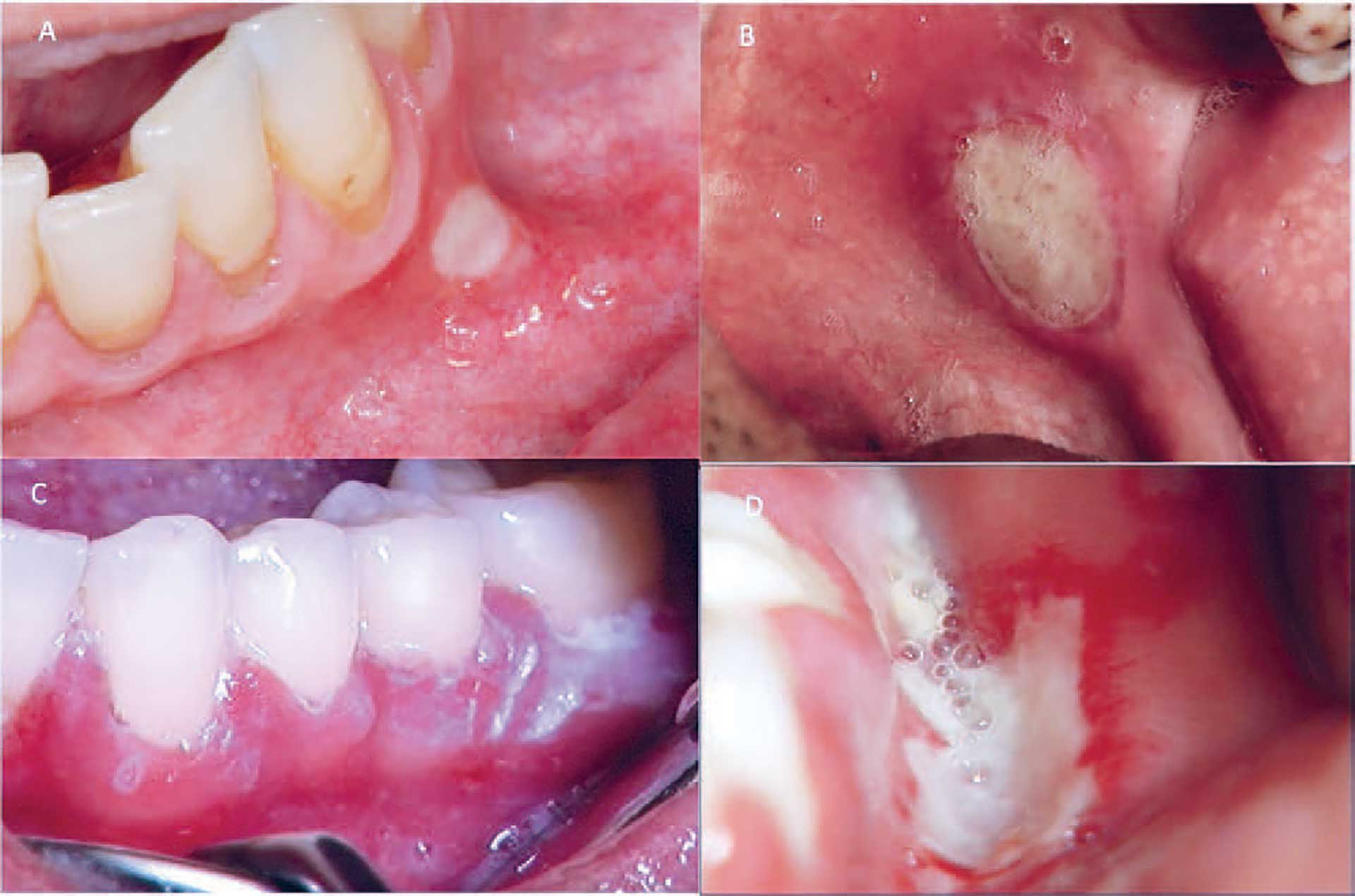
Fig. 2. A. Aftøs ulceration. B. Aftøs ulceration med ardannelse. C, D. Primær herpetisk gingivostomatitis.
Ved recidiverende intraorale herpes-associerede læsioner afficerer de små, bristede blister som regel det samme område af mundslimhinden, hyppigst ganeslimhinden (figur 3A). Læsionerne begynder som grupper af små vesikler, der brister og efterlader små cirkulære ulcerationer, der heler i løbet af 1–2 uger.
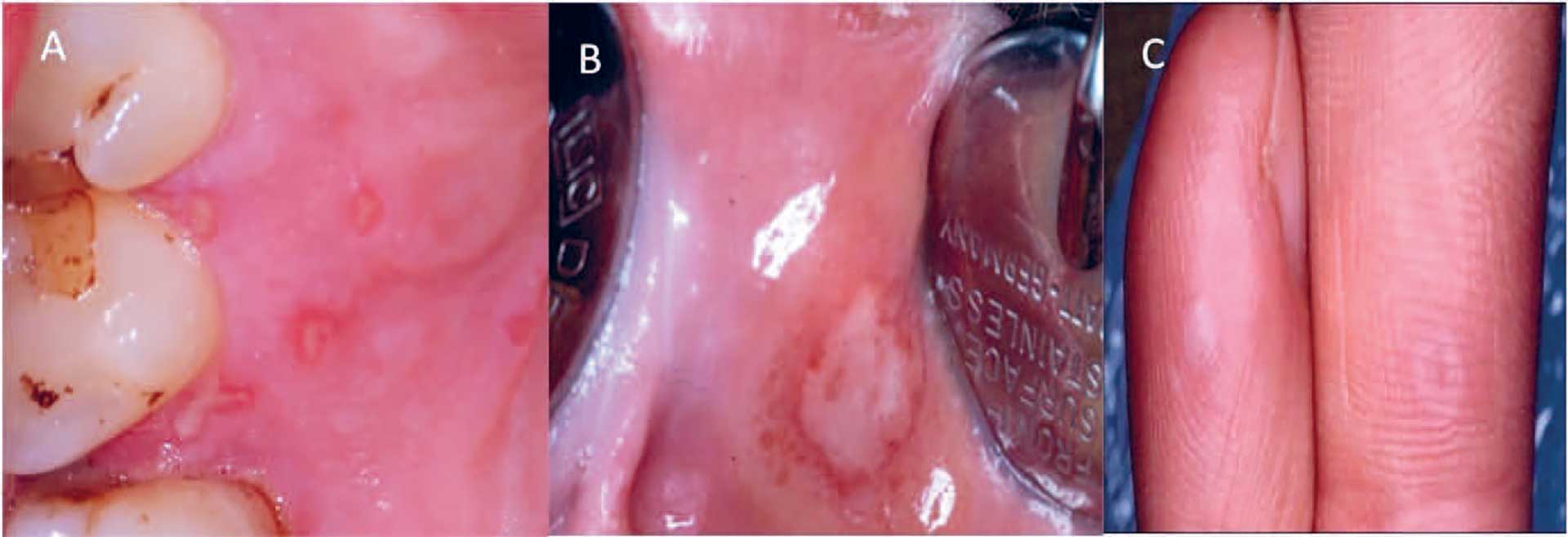
Fig. 3. A. Intraoral recidiverende herpes. B. Orale og C. kutane læsioner ved hånd-, fod- og mundsygdom.
Hånd-, fod- og mundsygdom (figur 3B) er en almindeligt forekommende virusinfektion, der skyldes coxsackie virus og som regel har et mildt forløb med let feber og få symptomer. Sygdommen rammer næsten udelukkende mindre børn og kan hos denne gruppe optræde med endemisk spredning, fx i børnehaver. Læsionerne afficerer typisk mundslimhinde, håndflader og fodsåler (figur 3C) [3]. Herpangina, som også skyldes coxsackie virus, er beslægtet med hånd-, fod- og mundsygdom, men forekommer sjældnere og er begrænset til den posteriore del af mundhulen, den bløde gane og tonsillerne, og ulcerationerne er ofte større (figur 4A); dertil kommer, at der ikke er læsioner på ekstremiteterne. Begge tilstande er sædvanligvis selvafgrænsende, og behandlingen er primært symptomlindrende [4]. Herpes zoster forekommer derimod unilateralt og er ledsaget af kraftig smerte. Også denne sygdom er karakteriseret ved bristende vesikler (figur 4B) [5].
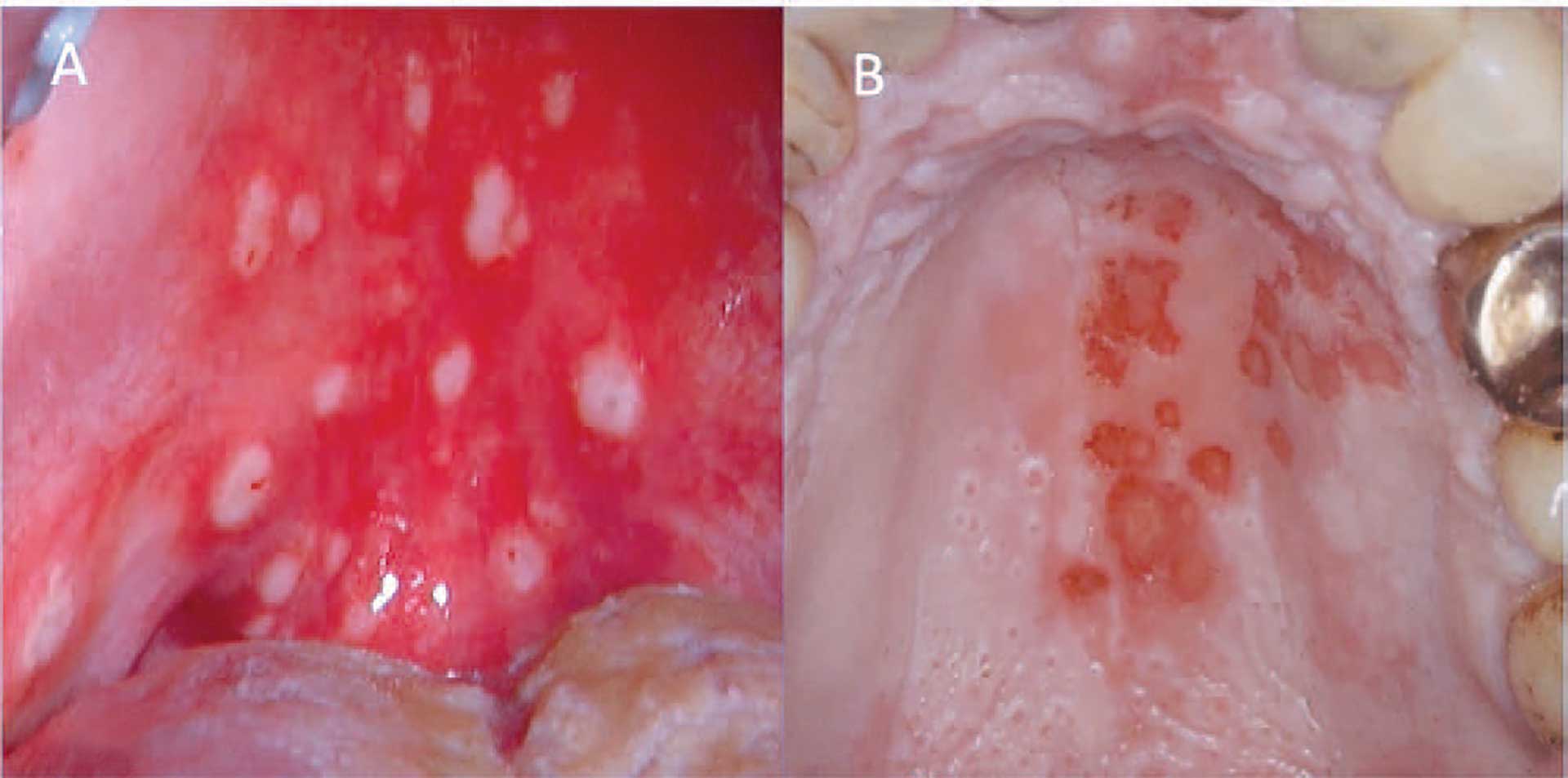
Fig. 4. A. Ulcerationer i ganen på grund af herpangina. B. Unilaterale bristende vesikler på grund af herpes zoster.
Ulcerøs oral lichen planus, tandbørsteskader, erythema multiforme og oral cancer
Uregelmæssige fibrindækkede ulcerationer er almindelige læsioner ved lichen planus (figur 5A). De kan afficere alle dele af mundslimhinden, findes ofte bilateralt og persisterer typisk i månedsvis. Den kliniske diagnose hviler på forekomst af hvide stregtegninger, som er det klassiske træk ved lichenoide læsioner. De hvide stregtegninger kan optræde i forbindelse med ulcerationerne eller andre steder i mundslimhinden (figur 5A) [6].
Tandbørsteskader i mundslimhinden afficerer ofte kun de mest prominerende områder af den fastbundne gingiva, men kan også forekomme på den tilstødende mundslimhinde (figur 5B). Læsionerne er typisk horisontalt orienterede, fordi de skyldes voldsom tandbørstning med horisontal teknik [7].
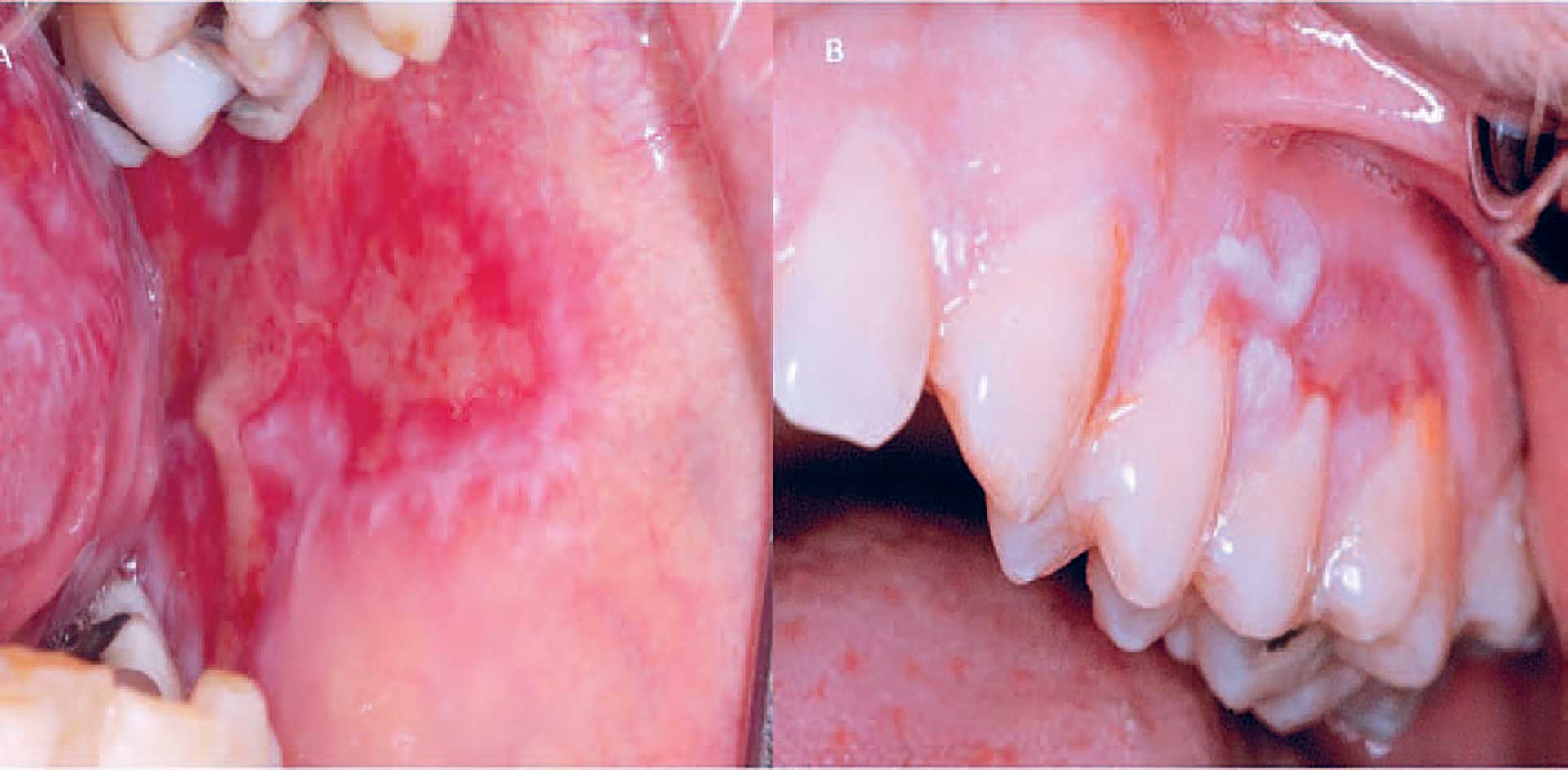
Fig. 5. A. Oral lichen planus. B. Tandbørstelæsioner på gingiva.
Oral erythema multiforme (OEM) er en sjælden, akut inflammatorisk sygdom, der afficerer mundslimhinden (figur 6A) og ofte recidiverer. OEM er karakteriseret ved spredte, uregelmæssige ulcerationer, som er dækket af et tykt fibrinlag. Hvis læberne afficeres, ses ofte skorpedannelse. OEM anses for at være en hypersensibilitetsreaktion, der udløses af visse lægemidler eller virusinfektioner [8]. Planocellulært karcinom er den hyppigst forekommende maligne tilstand i mundhulen, og det er derfor vigtigt at kunne identificere den. Tumoren kan udvise en ulcereret overflade, men dette er ikke altid tilfældet. Uregelmæssige, ofte palpable, eleverede rande og forekomst af røde eller hvide noduli er vigtige synlige tegn (figur 6B). Sent i forløbet ved disse tumorer vil der ofte forekomme smerte [9].
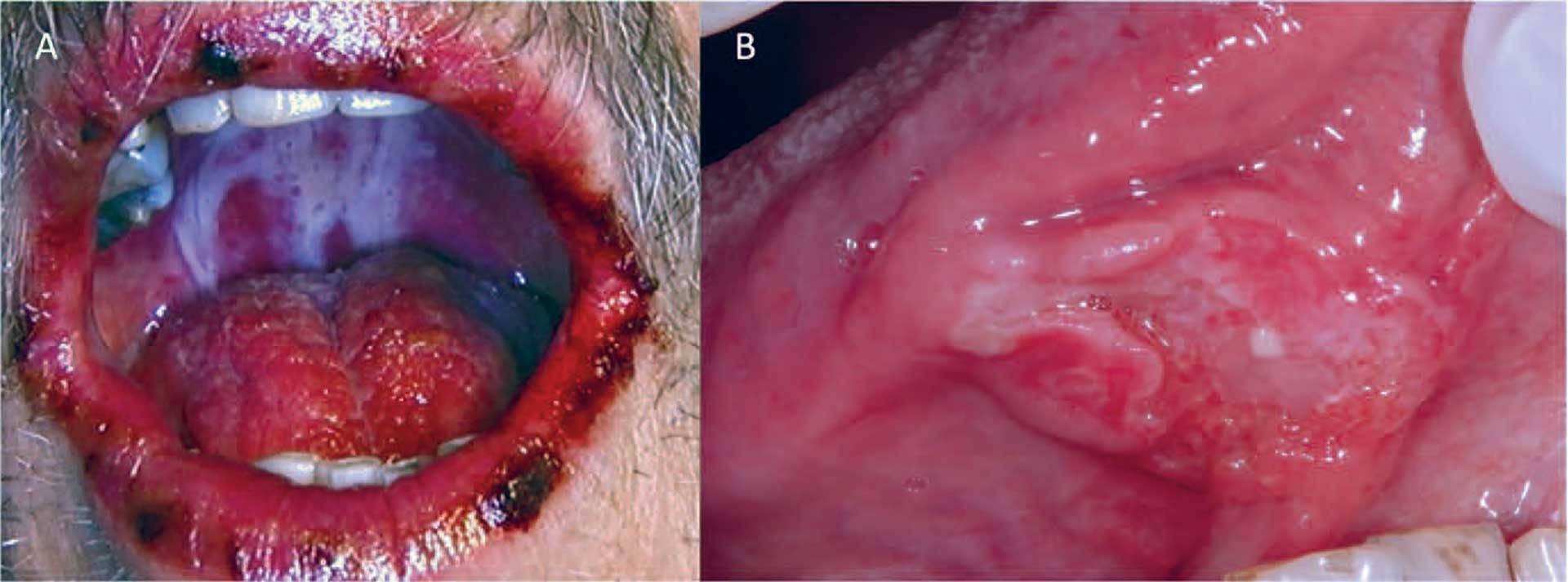
Fig. 6. A. Oral erythema multiforme. B. Oralt planocellulært carcinom.
Pemphigus vulgaris og slimhindepemfigoid
Den primære læsion af pemphigus vulgaris kan fremstå som en erosion med rødme som følge af tabet af de suprabasale epitelcellelag og er ofte omgivet af en mere hvidlig slimhinde (figur 7A). Tilstanden kan ses overalt i mundslimhinden [10]. Ved pemphigoid dannes bullae i slimhinden langs basalmembranen, og derfor ses ofte subepitelial blødning i læsionerne, der derved ses som hæmoragiske bullae typisk lokaliseret på gingiva (figur 7B). Blærerne har et tykkere låg, da de i modsætning til pemphigus involverer hele epitelet [11]. Hvis blærerne brister, kommer der fibrindækkede sår af varierende omfang. Pemphigus vulgaris optræder hyppigst i aldersgruppen 30-50 år og involverer typisk både mundslimhinde og hud, mens slimhindepemfigoid som regel debuterer senere i livet og stort set aldrig giver læsioner på huden.
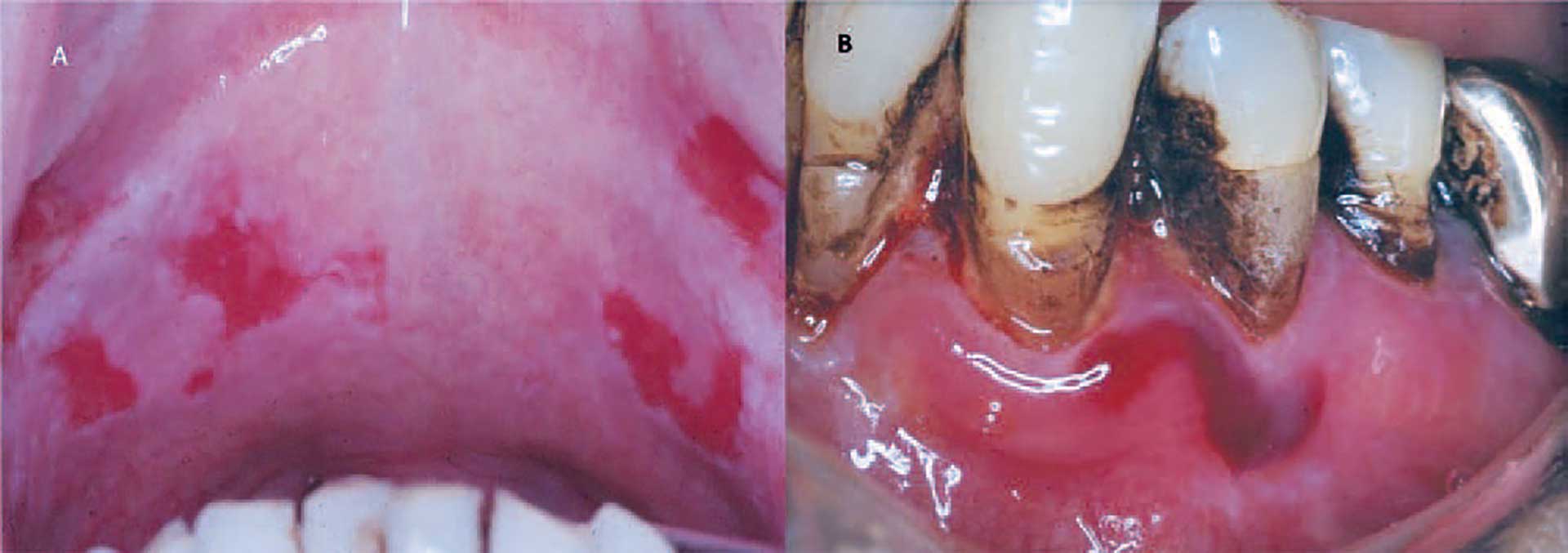
Fig. 7. A. Oral pemphigus vulgaris. B. Slimhindepemfigoid.
Hvidlige læsioner
Morsicatio, snuslæsioner, pseudomembranøs candidiasis, lichenoide tilstande og leukoplakier
Hvide forandringer kan ses i form af hvidlige pletter, papler, stregtegninger, noduli og pseudomembraner. Karakteristiske hvide pletter med en flosset og uregelmæssig overflade ses ved morsicatio [12] (figur 8A) og snuslæsioner [13] (figur 8B). Pseudomembraner er afskrabelige hvide papelagtige forandringer, som fx ses ved pseudomembranøs candidiasis [14] (figur 8C). Netværk af retikulære stregtegninger kan indgå i lichenoide kontaktlæsioner i forbindelse med amalgamfyldninger [15] (Fig. 9A). Papler og stregtegninger er karakteristiske træk ved papuløs og retikulær oral lichen planus (figur 9B) og optræder ofte samtidigt [6]. Læsioner med hvidlige pletter uden noduli er klassiske træk ved homogene leukoplakier (figur 9C), mens ikke-homogene leukoplakier både har hvidlige og røde områder med eller uden noduli (figur 9D) [16].
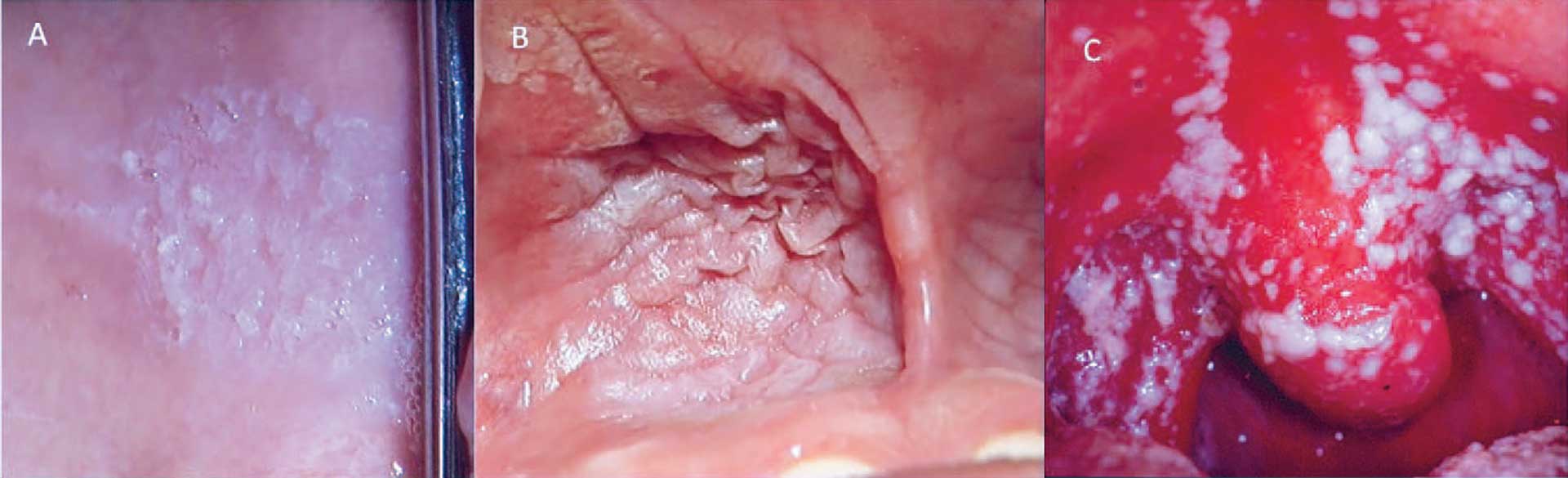
Fig. 8. A. Morsicatio i kindslimhinden. B. Snuslæsion i øvre omslagsfold. C. Pseudomembranøs candidiasis.
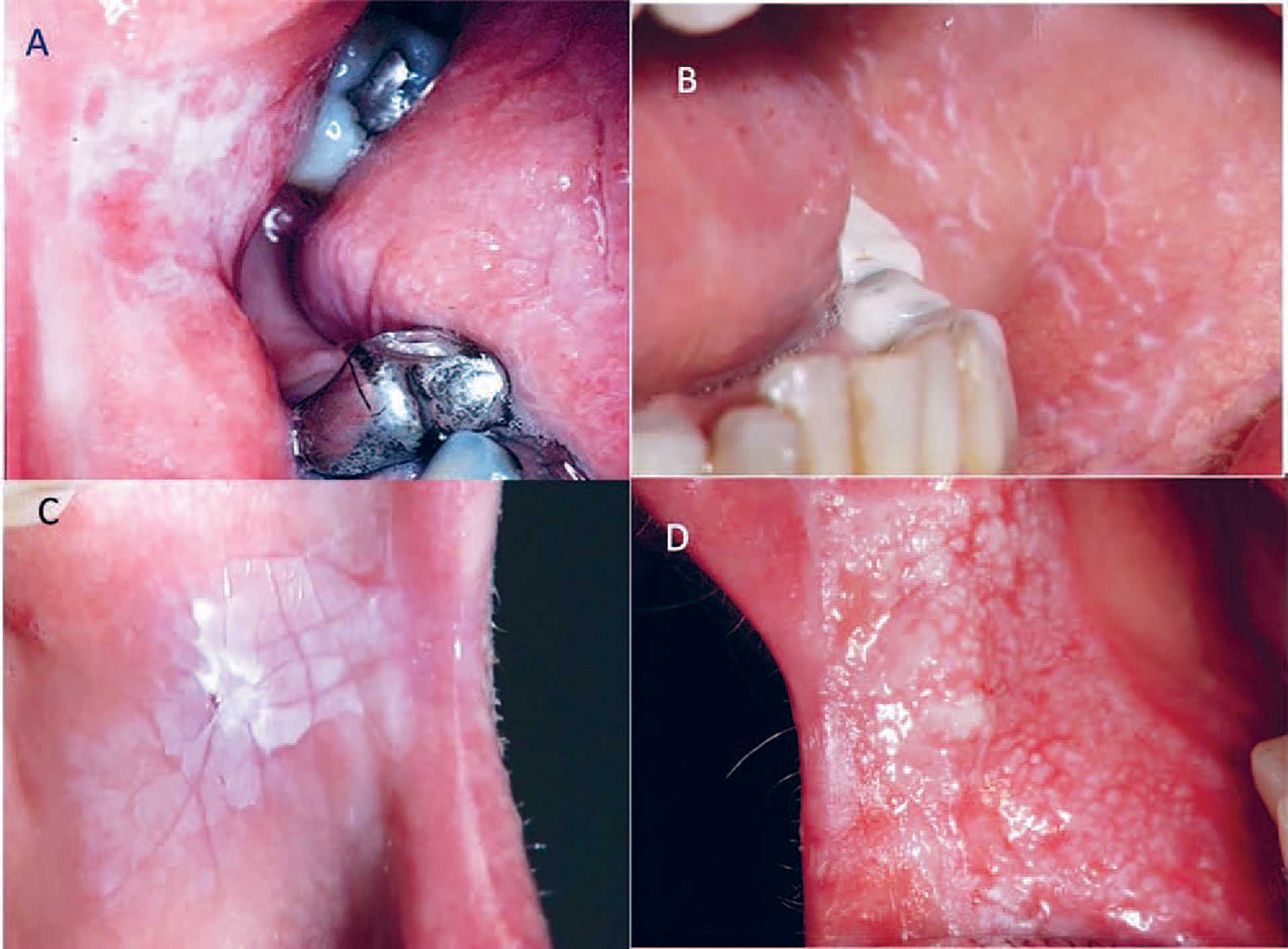
Fig. 9. A. Lichenoide kontaktlæsioner B. Oral lichen planus. C. Homogen leukoplaki D. Ikke-homogen leukoplaki.
Almindeligvis giver hvide læsioner ikke anledning til symptomer som smerte og ubehag, og i mange tilfælde bliver patienten først gjort opmærksom på læsionernes eksistens ved rutineundersøgelse hos tandlægen. Det bør understreges, at den endelige diagnose ofte først kan stilles efter biopsi, og dette gælder især for orale leukoplakier.
Erytematøse læsioner
Lingua geographica, hæmangiomer, erytematøs candidiasis, erytematøs lichen planus, discoid lupus erythematosus og erytroplaki
Lingua geographica er ofte omgivet af en gullig rand, og læsionerne ændrer konstant størrelse og udstrækning, for i perioder helt at forsvinde [17] (figur 10A). Rødme af slimhinden skyldes ofte atrofi af epiteldækket og inflammation, men kan også forekomme som følge af proliferation af kar, som det ses ved vaskulære tilstande som »hæmangiomer«, en samlebetegnelse for almindelige venøse malformationer og medfødte hæmangiomer [18]. Det er karakteristisk for sådanne forandringer, at de mister farve, hvis man trykker på overfladen (figur 10B). Hvor hæmangiomer som regel er symptomløse, vil de øvrige omtalte røde læsioner ofte medføre smerte eller ubehag, som regel på grund af det atrofiske epiteldække.
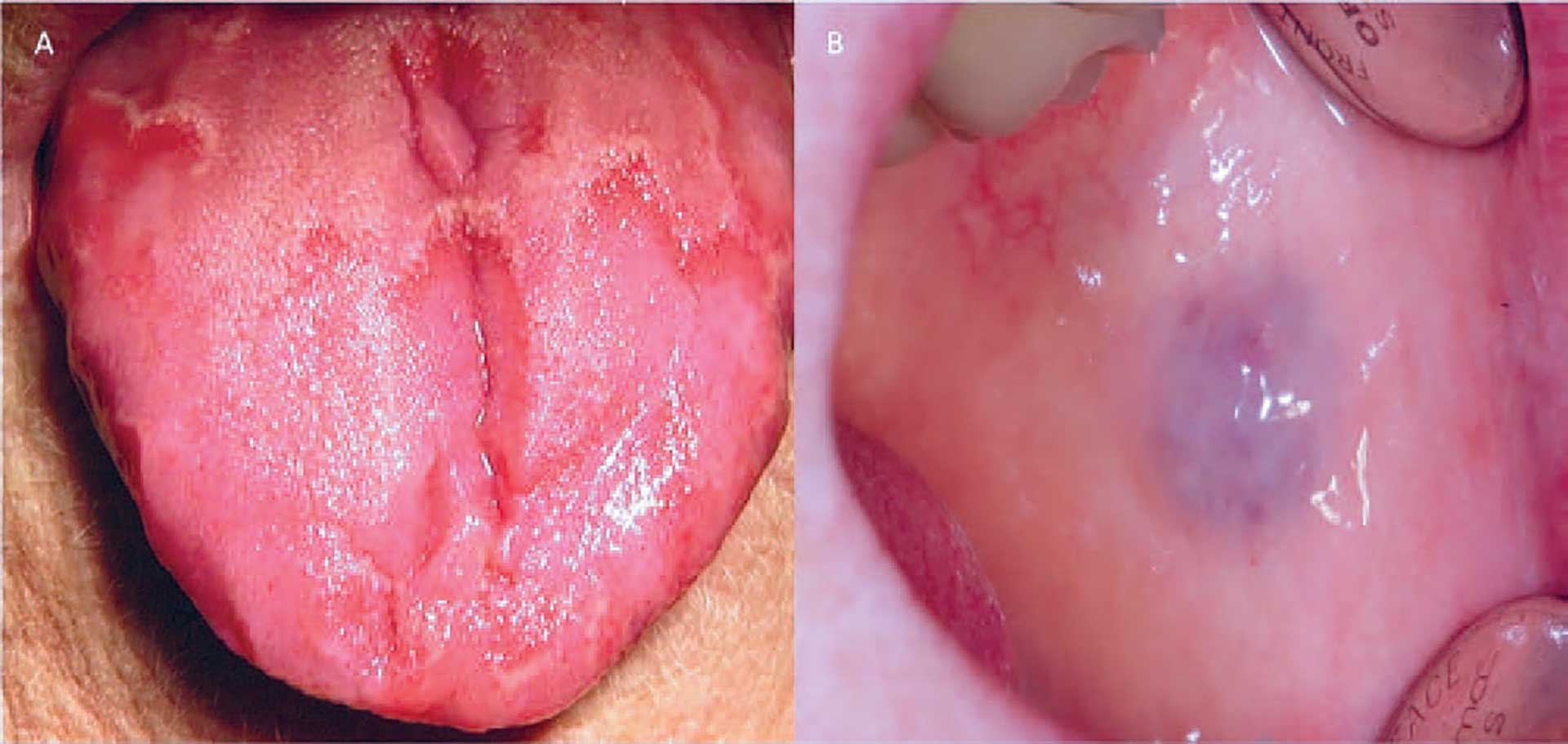
Fig. 10. A. Lingua geographica. B. Hæmangiom på kindslimhinden.
Diffuse røde områder ses ved erytematøse Candida-infektioner [14] (figur 11A). Røde forandringer er også det vigtigste træk ved erytroplaki, hvor det afficerede område ofte ligger en smule lavere end den omgivende slimhinde, som den som regel er skarpt afgrænset fra [19] (figur 11B). Læsionerne kan give anledning til ubehag eller decideret smerte, især i forbindelse med spisning. Den skarpe afgrænsning er i modsætning til situationen ved atrofiske lichenoide læsioner, hvor afgrænsningerne er diffuse og ofte ledsaget af hvide stregtegninger i grænseområderne og andre steder i mundslimhinden. Sommetider kan atrofiske læsioner også afficere gingiva, hvor de, i modsætning til almindelig gingivitis, ofte efterlader bleg margo gingivae uden rødme (figur 11C). Ved discoid lupus erythematosus er det klassiske træk en rød læsion med irradierende fine stregtegninger og små papler [20] (figur 11D).
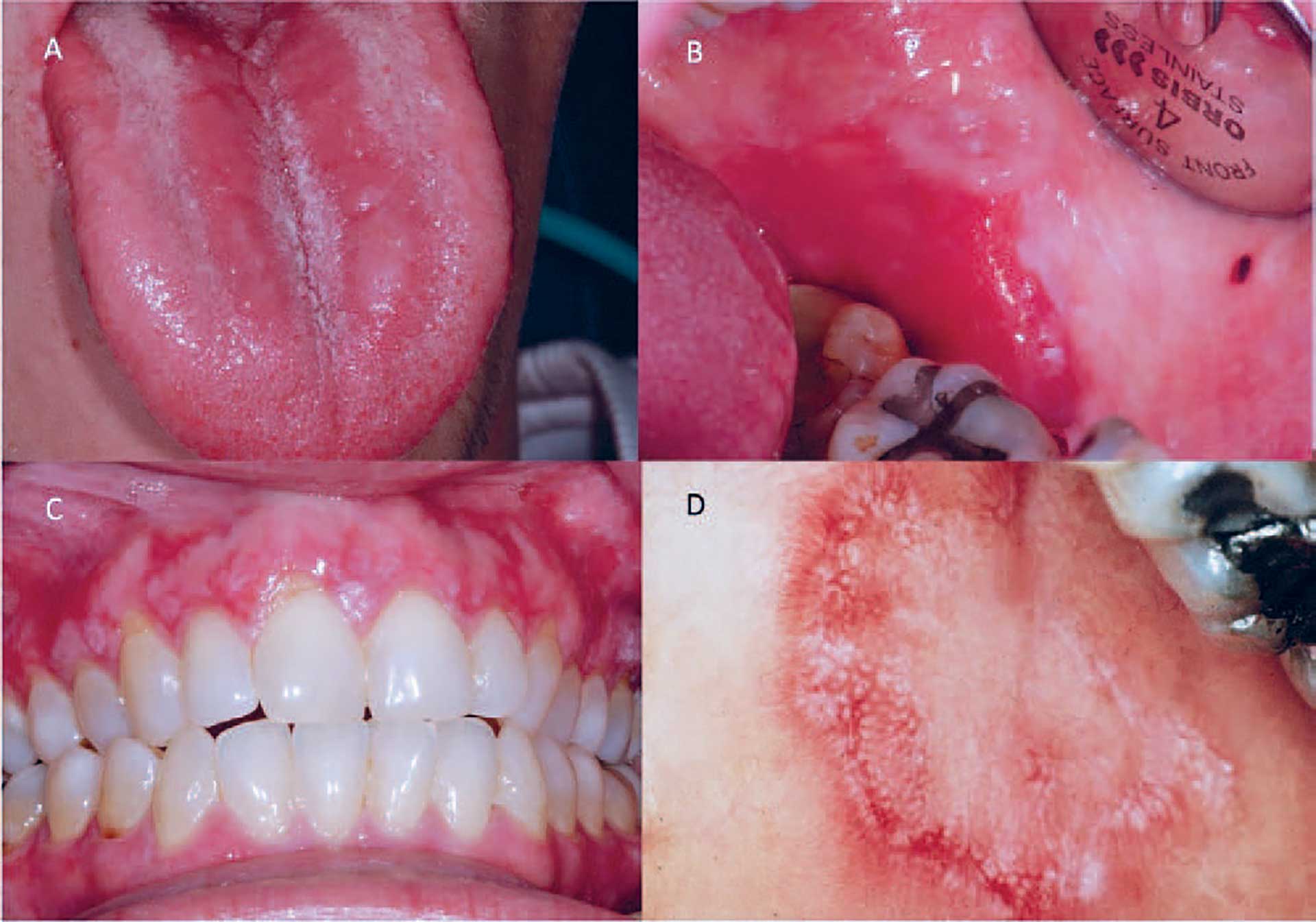
Fig. 11. Erytematøs candidiasis. B. Erytroplaki. C. Atrofiske lichenoide læsioner på gingiva. D. Discoid lupus erythematosus.
Pigmenterede læsioner
Amalgamtatovering, melanotisk macula, melanocytisk naevus, lægemiddel-induceret pigmentering, postinflammatorisk pigmentering, rygermelanose, Mb. Addison, Peutz–Jeghers syndrom og malignt melanom
En almindelig årsag til slimhindepigmentering er amalgamtatovering (figur 12A), hvor små eller større amalgampartikler aflejres i slimhinden efter iatrogen beskadigelse af epitelet. Derfor fremtræder tilstanden typisk med en blålig eller grålig farve og ofte med et ar centralt i læsionen [21].
Den orale melanotiske macula er en lille brun/sort pigmentering, der oftest ses på læberne (Fig. 12) og gingiva. Melanocytisk naevus, der sjældent forekommer i mundslimhinden, svarer til modermærker på huden og er små let eleverede blå/brune områder, der typisk ses i ganeslimhinden [21][22]. Blåt naevus klassificeres som en form for melanocytisk naevus (figur 12C).
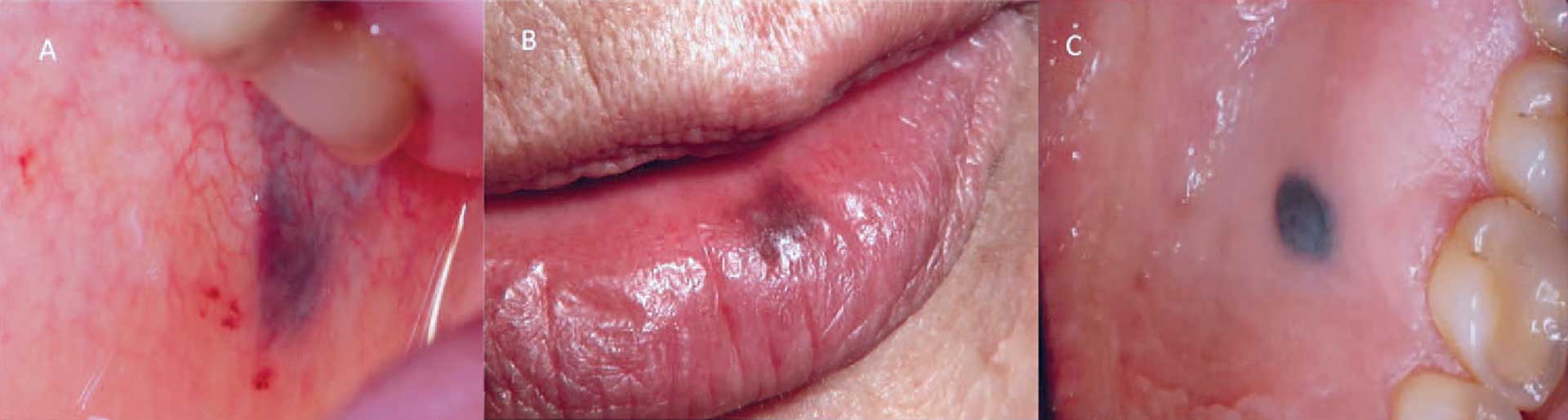
Fig. 12. A. Amalgamtatovering. B. Oral melanotisk macula. C. Blåt naevus.
Lægemiddel-induceret pigmentering kan fremkaldes af lægemidler som antimalariamedicin, antibiotika og kemoterapeutika. Imatinib er et relativt nyt målrettet middel mod cancer og kan forårsage pigmentering i ganen (figur 13A). Postinflammatorisk pigmentering ses hyppigst hos patienter med mørk hudfarve. I figur 13B ses en patient med retikulær oral lichen planus, som har udviklet et pigmenteret retikulært netværk. Storrygere har risiko for rygermelanose, der ofte optræder som en generaliseret pigmentering af de gingivale væv (figur 13C). Patienter med mørk hudfarve kan vise lignende pigmentering. Fysiologisk pigmentering i mundslimhinden er almindeligt forekommende, men diffuse pigmenterede områder kan skyldes sygdomme som Mb. Addison (figur 13D) og Peutz–Jeghers syndrom (figur 13E). Disse sygdomme er sjældne og viser også hyperpigmentering af huden [22].
Oralt malignt melanom (OMM) (figur 13F) er en alvorlig, men yderst sjælden mundslimhindesygdom, der fremstår som en sortbrun plet med intern farvevariation. OMM forekommer hyppigst i ganeslimhinden og er hurtigt progredierende. Tidlig diagnostik er vigtig, da OMM har dårlig prognose – dårligere end tilsvarende læsioner på huden.
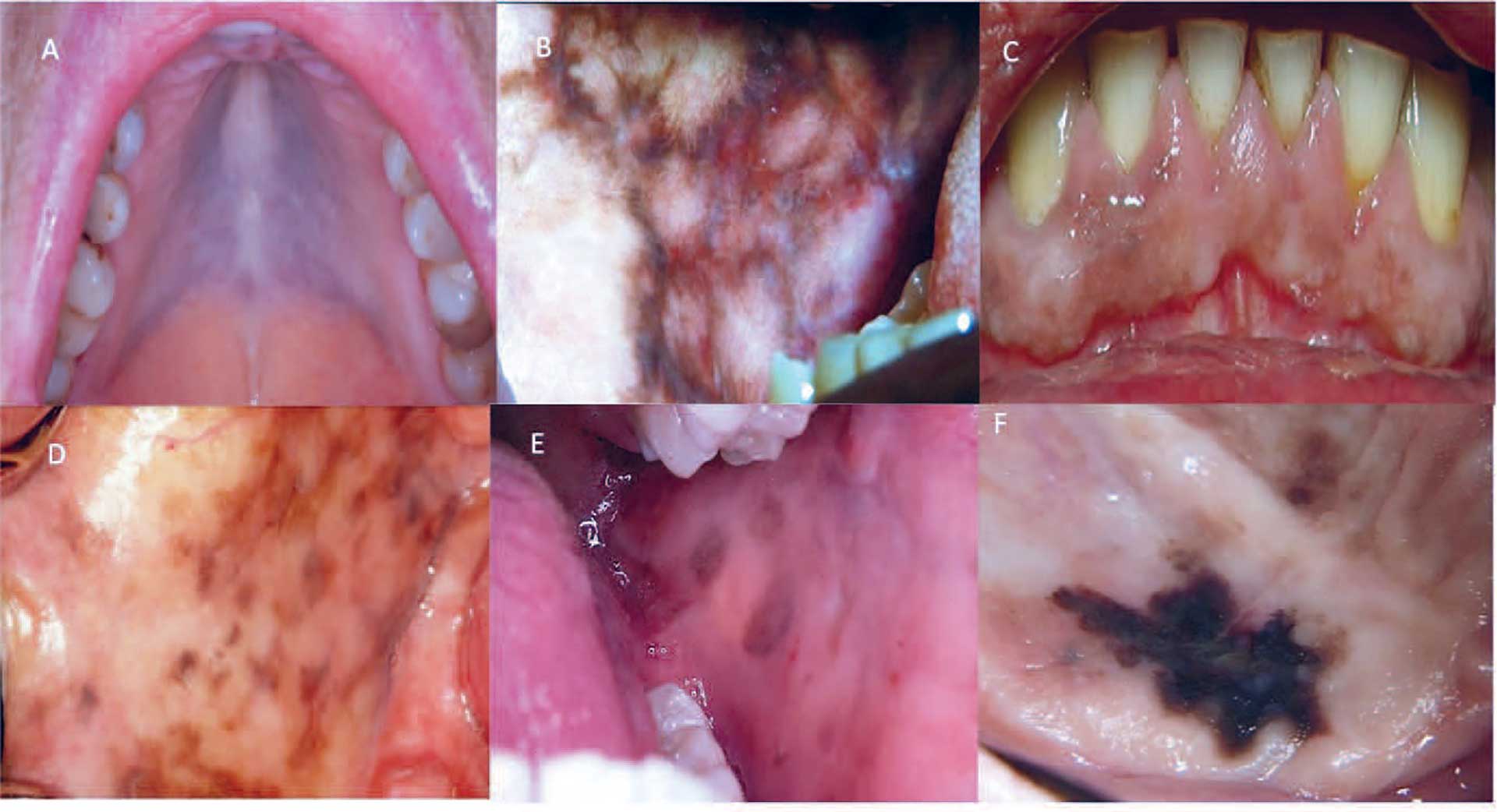
Fig. 13. A. Lægemiddel-induceret pigmentering. B. Pigmenteret retikulær oral lichen planus. C. Rygermelanose. D. Pigmentering ved Morbus Addison. E. Pigmentering ved Peutz-Jeghers syndrom. F. Oralt malignt melanom.
Læsioner med vævstilvækst
Fibroepitelial hyperplasi, pyogent granulom, carcinom og lymfom
Fibroepitelial hyperplasi afficerer ofte gingiva, men kan forekomme andre steder i mundslimhinden. Tilstanden er karakteriseret ved en glat, bleg eller let erytematøs overflade (figur 14A). Pyogene granulomer rammer også hyppigt gingiva, men har en tydeligt rød overflade på grund af rig vaskularisering. Der forekommer ofte ulcererede fibrindækkede områder (figur 14B). Spytkirtelkarcinomer og lymfomer ligger derimod ofte dybt i vævet, og slimhindedækket er intakt [23][24].
Planocellulært karcinom kan fremtræde som en hævelse af regelmæssig eller oftest uregelmæssig form med eller uden ulceration (figur 14C). Tumoren kan give anledning til smerte og, hvis processus alveolaris er involveret, desuden displacering af tænder. Det er vigtigt at påpege, at tumorer i ganen meget ofte er maligne spytkirteltumorer eller lymfomer (figur 14D), hvilket man skal have in mente ved udredning og behandling [25].
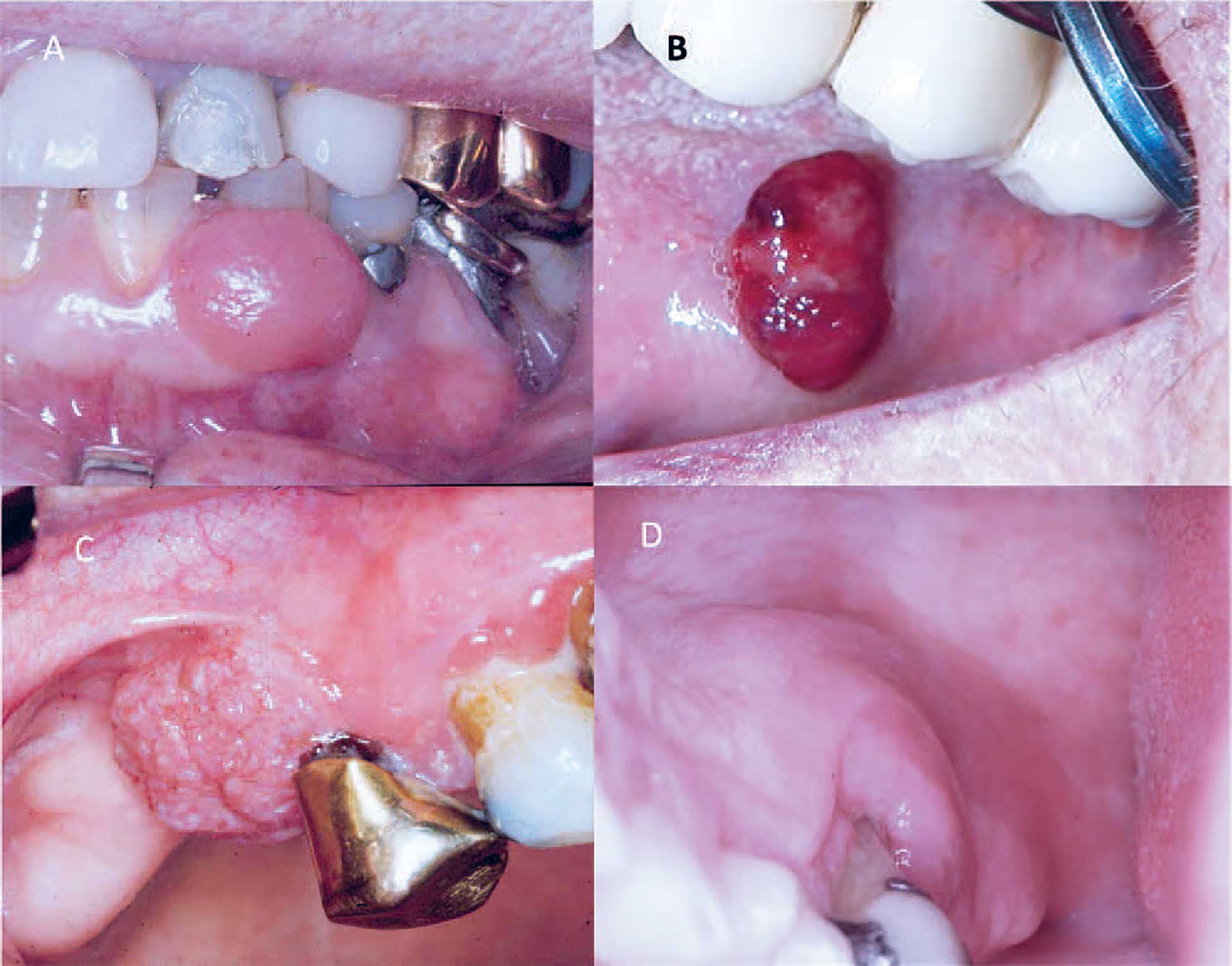
Fig. 14. A. Fibroepitelial hyperplasi. B. Pyogent granulom. C. Planocellulært karcinom. D. Slimhindehævelse ved lymfom.
Litteratur
Arduino PG, Porter SR. Oral and perioral herpes simplex virus type 1 (HSV-1) infection: review of its management. Oral Dis. 2006;12:254-70.
Scully C, Porter S. Oral mucosal disease: recurrent aphthous stomatitis. Br J Oral Maxillofac Surg. 2008;46:198-206.
Leung AKC, Lam JM, Barankin B et al. Hand, foot, and mouth disease: a narrative review. Recent Adv Inflamm Allergy Drug Discov. 2022;16:77-95.
Légeret C, Furlano R. Oral ulcers in children - a clinical narrative overview. Ital J Pediatr. 2021;47:144.
Mohan RP, Verma S, Singh U et al. Herpes zoster. BMJ Case Rep. 2013;2013: bcr2013010246.
Thorn JJ, Holmstrup P, Rindum J et al. Course of various clinical forms of oral lichen planus. A prospective follow-up study of 611 patients. J Oral Pathol. 1988;17:213-8.
Ranzan N, Muniz FWMG, Rosing CK. Are bristle stiffness and bristle end-shape related to adverse effects on soft tissues during toothbrushing? A systematic review. Int Dent J. 2019;69:171-82.
Samim F, Auluck A, Zed C et al. Erythema multiforme: a review of epidemiology, pathogenesis, clinical features, and treatment. Dent Clin North Am. 2013;57:583-96.
Montero PH, Patel SG. Cancer of the oral cavity. Surg Oncol Clin N Am. 2015;24:491-508.
Scully C, Challacombe SJ. Pemphigus vulgaris: update on etiopathogenesis, oral manifestations, and management. Crit Rev Oral Biol Med. 2002;13:397-408.
Petruzzi M. Mucous membrane pemphigoid affecting the oral cavity: short review on etiopathogenesis, diagnosis and treatment. Immunopharmacol Immunotoxicol. 2012;34:363-7.
Sewerin I. A clinical and epidemiologic study morsicatio buccarum-labiorum. Scand J Dent Res. 1971;79:73-80.
Andersson G, Axéll T. Clinical appearance of lesions associated with the use of loose and portion-bag packed Swedish moist snuff: a comparative study. J Oral Pathol Med. 1989;18:2-7.
Holmstrup P, Axéll T. Classification and clinical manifestations of oral yeast infections. Acta Odontol Scand 1990;48:57-9.
Bolewska J, Hansen HJ, Holmstrup P. et al. Oral mucosal lesions related to silver amalgam restorations. Oral Surg Oral Med Oral Pathol. 1990;70:55-8.
Holmstrup P, Vedtofte P, Reibel J et al. Long-term treatment outcome of oral premalignant lesions. Oral Oncol 2006;42:461-74.
Dafar A, Cevik-Aras H, Robledo-Sierra J et al. Factors associated with geographic tongue and fissured tongue. Acta Odontol Scand. 2016;74:210-6.
Bonet-Coloma C, Minguez-Martinez I, Palma-Carrio C et al. Clinical characteristics, treatment and outcome of 28 oral haemangiomas in pediatric patients. Med Oral Patol Oral Cir Bucal. 2011;16:e19-22.
Holmstrup P, Plemons J, Meyle J. Non-plaque-induced gingival diseases. J Periodontol. 2018;89 (Supp 1):S28-45.
Schiødt M. Oral manifestations of lupus erythematosus. Int J Oral Surg. 1984;13:101-47.
Rosebush MS, Briody AN, Cordell KG. Black and brown: Non-neoplastic pigmentation of the oral mucosa. Head Neck Pathol. 2019;13:47-55.
Gondak RO, da Silva-Jorge R, Jorge J et al. Oral pigmented lesions: Clinicopathologic features and review of the literature. Med Oral Patol Oral Cir Bucal. 2012;17:e919-24.
Brierley DJ, Crane H, Hunter KD. Lumps and bumps of the gingiva: A pathological miscellany. Head Neck Pathol. 2019;13:103-13.
Vasanthi V, Divya B, Ramadoss R et al. Quantification of inflammatory, angiogenic, and fibrous components of reactive oral lesions with an insight into the pathogenesis. J Oral Maxillofac Pathol. 2022;26:600.
Holmstrup P, Jontell M. Non-plaque-induced gingival diseases. In: Berglundh T, Giannobile WV, Lang NP et al, eds. Clinical periodontology and implant dentistry. 1. Seventh ed. Oxford, UK: John Wiley & Sons, Ltd., 2022;331-67.
English summary
et al.
Differential diagnosis of oral mucosal diseases
Nor Tannlegeforen Tid. 2024; 134: 138-44.
It is evident that a prerequisite for the management and treatment of oral mucosal diseases is reaching a correct diagnosis. However, in general dental practice, oral mucosal diseases are not sufficiently common to establish a routine. This is why such diseases may be difficult to diagnose, and the purpose of the present article is to briefly present clinical tools for clinicians to discriminate between various lesions with similar clinical features, i.e., ulcerative/vesicular/bullous lesions, changes in colour, including white, erythematous, and pigmented lesions, and lesions with tissue overgrowth.
The frame of this article does not allow a presentation of all oral mucosal diseases and therefore is limited to some of those presented in the previous article, which are of most relevance in daily practice.
Korrespondanceansvarlig sjetteforfatter: Palle Holmstrup, E-mail adresse: pah@sund.ku.dk
Accepteret til publikation den 2. september 2023. Artikkelen er refereevurdert
Rautava J, Bankvall M, Gjerde CG, Jontell M, Dabelsteen E, Holmstrup P, et al. Oversigtsartikel. Differentialdiagnostik af mundslimhindesygdomme. Nor Tannlegeforen Tid. 2024; 134: 138-44.
Emneord: Mouth; oral mucosa; oral medicine; differential diagnostics
