Per Einar Dagsson Myklebust, Magnus Fossgård og Inge Fristad
Natrium-hypo-kloritt og vevs-oppløselighet
Tannlege. DOT, Vestland fylkeskommune, Bergen
Tannlege. DOT, Rogaland fylkeskommune, Stavanger
Professor. Institutt for klinisk odontologi, Det medisinske fakultet, Universitetet i Bergen
Hovedbudskap
NaOCl-løsninger leveres i hovedsak i ubufret form, og ofte i høye konsentrasjoner
De antibakterielle egenskapene øker ved bufring, mens de vevsoppløsende og toksiske egenskapene øker med økt konsentrasjon
Bufring av NaOCl-løsninger anbefales for å optimalisere de antibakterielle egenskapene
Samtidig vil bufring også redusere de vevstoksiske egenskapene
Hensikten med denne studien var å se på vevsoppløsende egenskaper og pH for noen kommersielt tilgjengelige løsninger av natriumhypokloritt (NaOCl). Ved hjelp av preparater fra muskelvev hos gris ble de vevsoppløsende egenskapene illustrert i bufret og ubufret tilstand over en tidsperiode på 60 minutt. Samtlige løsninger forelå i ubufret tilstand og ble derfor bufret før forsøket. De vevsoppløsende egenskapene var mer avhengig av konsentrasjon enn pH, selv om forskjellene ikke var vesentlige. I klinisk praksis er det viktig å balansere de vevsoppløselige egenskapene opp mot vevsvennlighet og de antibakterielle egenskapene. Produsentene av de kommersielt tilgjengelige NaOCl-løsninger synes å ha et ensidig fokus på holdbarhet framfor vevsvennlighet og antibakteriell effekt.
Natriumhypokloritt (NaOCl) er et salt som løst i vann er sterkt oksiderende. Løsningen benyttes til desinfisering og bleking. Til endodontisk bruk har ulike alternative irrigasjonsmidler blitt lansert, men NaOCl-løsninger er stort sett enerådende på grunn av kombinasjonen av de desinfiserende og vevsoppløsende egenskapene [1]. NaOCl-løsninger leveres i ulike konsentrasjoner, og bufring vil redusere den vevstoksiske effekten som er høy for de ubufrede og svært basiske løsningene. Den antibakterielle og vevsoppløsende effekten til NaOCl-løsninger vil være avhengig av konsentrasjon og surhetsgrad (pH) [1][2][3][4][5][6].
Apotekene stod tidligere for distribusjon og salg av NaOCl-løsninger til odontologisk bruk. Dette forandret seg etter endring av apotekloven i 2010. Dentale depoter står nå fritt til å selge kommersielle løsninger, og de fleste er ubufrede løsninger med høy pH. Grunnen til dette har nok sammenheng med holdbarheten knyttet til disse [3][6]. Dette underbygges av hva som et tilgjengelig hos ulike dentalleverandører, der ubufrede løsninger i konsentrasjoner opp mot 6 % tilbys i Norge.
Vevsvennlighet og vevsoppløsende egenskaper er to motstridende ønsker, siden vevsvennlighet avtar når de vevsoppløselige egenskapene øker [1]. Både bufring og lavere konsentrasjon på NaOCl-løsninger vil påvirke vevsvennlighet positivt. De antibakterielle egenskapene øker også betraktelig ved bufring på grunn av mer tilgjengelig HOCL [3][6][7] En bufret lav konsentrasjon vil derfor kunne ha like god antibakteriell effekt som en ubufret høy konsentrasjon. Det eneste argumentet som skulle forsvare bruk av høyere konsentrasjoner er de vevsoppløselige egenskapene. Men, ved uønskede hendelser, hvor sterk ubufret NaOCl-løsning presses ut periapikalt eller ved sprut mot øynene, kan dette medføre alvorlige og permanente skader [8][9]. Det kan derfor være uheldig at medikamenter med en mulig vevsødeleggende effekt, skal gå veien utenom apotekene hvor tannlegene kan få kvalifiserte råd og anbefalinger [6]. I dag kreves CE-merking som innebærer at det er produsentens ansvar å registrere meldinger om uønskede hendelser og treffe relevante tiltak.
Denne studien har til hensikt å illustrere om de vevsoppløselige egenskapene endres drastisk ved økt konsentrasjon, og om disse påvirkes nevneverdig av bufring.
Materiale og metode
Vevspreparater og forsøksprotokoll
Organisk materiale til vevspreparater ble hentet fra grisekjever som benyttes ved kirurgisk trening i studentklinikken. Preparatene ble laget med en biopsistanser (Sterile Disposable Biopsy Punch, 4 mm, Miltexâ) fra tynne skiver av muskelvev, med en vekt tilsvarende pulpavev i en flerrotig tann [1][2]. Preparatene ble veid med en laboratorievekt (AG204 DeltaRange, Mettler Toledo, Malaysia).
Syv milliliter av bufrede og ubufrede NaOCl-løsninger i konsentrasjon 1 % (Sykehusapotekene HF), 3 % (CanalPro, Coltene Group), samt vanlig 5 % husholdningsklor (Klor, Rema1000, Rema Koin AS) ble benyttet. Bufring ble gjort ved titrering med natriumbikarbonat for at konsentrasjonen skulle være upåvirket. Løsningene ble tilsatt petriskåler (Petri Dishes Disposable, Avantorâ, USA), hvor vevspreparatene deretter ble plassert. Preparatene ble holdt under konstant bevegelse med en ristemaskin (Dual-Action Shaker KL 2, Edmund Bühler GmbH, Tyskland) ved 37°C.
Etter at preparatene var plassert i de ulike NaOCl-løsningene ble vevspreparatene fotografert (MC170 HD, Leica Microsystems, Tyskland) på et stereomikroskop (M205C, Leica Microsystems, Tyskland) etter et standardisert oppsett hvert kvarter inntil preparatene var oppløst i væsken.
Resultater
Vevspreparater
På tross av en standardisert metode for fremstilling viste resultatene av målingene noe variasjon i vekt mellom de ulike preparatene (gjennomsnitt 16,683 mg ± 0,366).
Konsentrasjon av NaOCl-løsninger
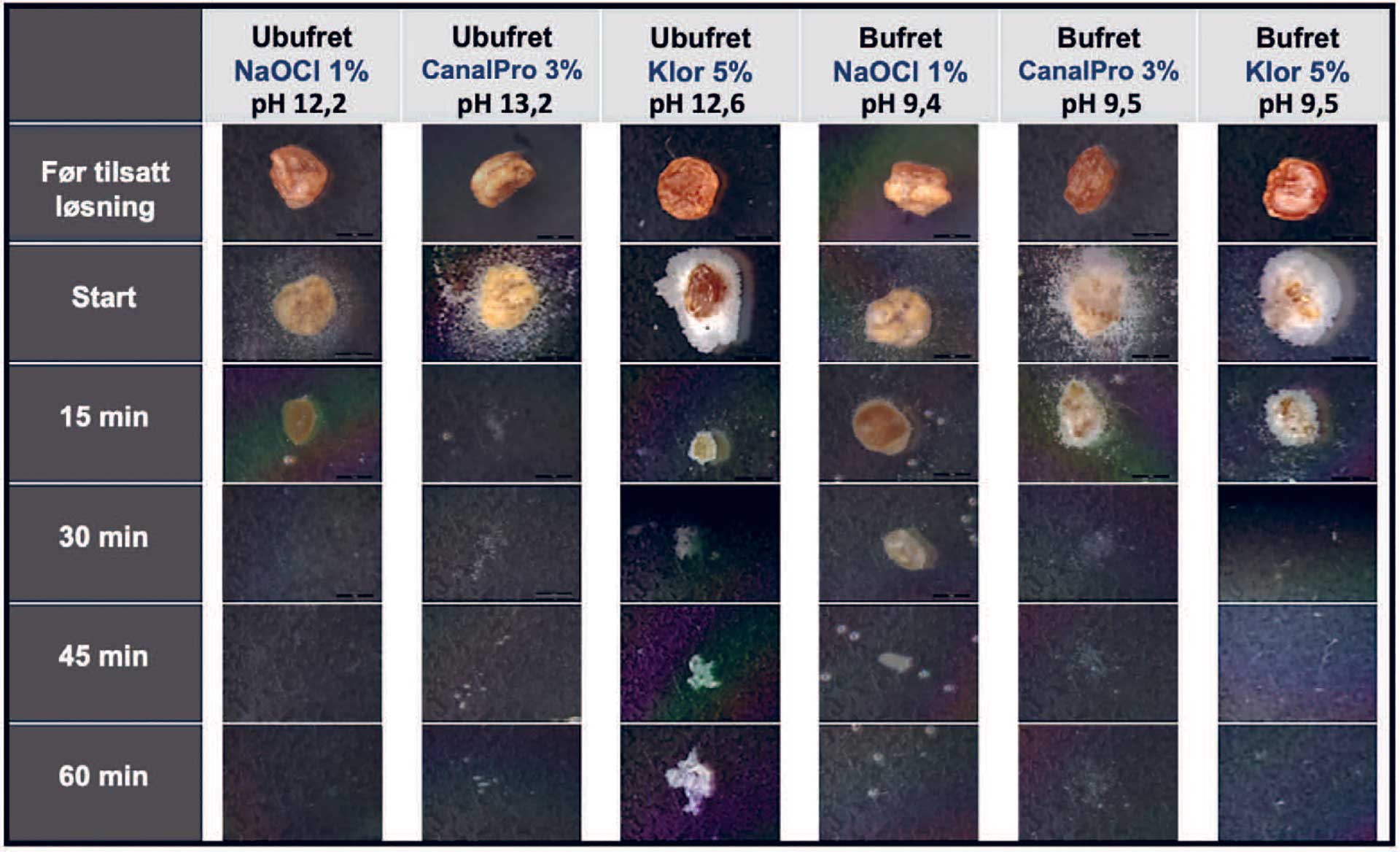
Figur 1. Bildene illustrerer effekten av ulike løsninger på vevsoppløselighet. De første tre kolonnene viser effekten av ubufret natriumhypokloritt i tre forskjellige konsentrasjoner (1, 3 og 5 %). De neste tre kolonnene viser effekten av de samme løsningene i bufret tilstand.
Figur 1 gir en oversikt over konsentrasjon og målt pH på de bufrede og ubufrede NaOCl-løsningene som ble benyttet.
Vevsoppløselighet
Bilder fra forsøket ble satt opp i serier i en tabellform for å illustrere forskjeller i vevsoppløselighet for de ulike løsningene (figur 1). På horisontalaksen ser vi de seks preparatene i tilhørende løsninger, mens tiden ved fotografering er vist på vertikalaksen. Figuren viser visuelt forskjeller på vevsoppløselighet for de ulike løsningene i bufret og ubufret tilstand. Start-bildene viser tydelig den initiale reaksjonen med umiddelbar gassdannelse, der det er liten forskjell mellom ubufrede og bufrede løsninger. Generelt er det relativt lite som skiller de bufrede og ubufrede løsningene når det gjelder vevsoppløselighet. Samtidig er det en tendens til at vevsoppløseligheten øker med konsentrasjon, men alle løsningene har en relativt god vevsoppløsende effekt.
Diskusjon
I studien ønsket vi å få fram forskjeller på vevsoppløsende effekt, både i forhold til konsentrasjon og bufring. Til dette ble det benyttet preparater tilsvarende vekten på pulpavev i en molar [10][11]. I en klinisk situasjon vil mesteparten av vevet fjernes mekanisk, samtidig som gjenværende vev er delvis oppløst og med stor tilgjengelig overflate for kjemisk nedbrytning. Det er derfor rimelig å anta at en med god gjennomskylling og fornying av irrigasjonsvæsken, for å motvirke inaktivering i kanalen, kan oppnå lavere nedbrytningstid. Vi ser at 7 ml NaOCl-løsning er tilstrekkelig for fullstendig oppløsning av vevet. Tidsbruken varierte fra et sted mellom 0-15 minutter for den mest effektive (CanalPro 3 % ubufret), til omkring 45 minutter for de minst effektive (1 % bufret og 5 % ubufret). Resultatene indikerer at de ubufrede løsningene generelt er noe mer vevsoppløsende enn tilsvarende bufrede løsninger, uten at vevsoppløseligheten er dramatisk påvirket. Dette viser at både pH og konsentrasjon spiller en viss rolle for NaOCl-løsningene sine vevsoppløsende egenskaper i forsøket. I en klinisk sammenheng vil oppvarming av NaOCl-løsningene øke de antibakterielle og vevsoppløsende egenskapene [12][13][14].
Forskjeller i vevsoppløselighet for 5,25 % og 2,6 % NaOCl-løsninger med pH 6, 9 og 12 har tidligere vært målt i opptil 30 minutter [5]. Det ble ikke funnet signifikant forskjell mellom løsningene med pH 9 og 12. Vår studie viste at 3 %-løsningen CanalPro brukte kortere tid enn en 5 %-løsning i ubufret tilstand. Dette kan bero mer på pH enn konsentrasjon, siden vevsoppløseligheten var omtrent lik i bufret tilstand. Siden forsøket var ment som en visuell illustrasjon av effekten av pH og konsentrasjon, må en imidlertid være varsom med å trekke kvantitative konklusjoner.
For de ubufrede løsningene i forsøket varierte pH-verdiene fra 12,2 til 13,1. Siden pH-skalaen er logaritmisk, vil det tilsvare en økning i basisitet på nesten 10 ganger. Det kan synes rart at 3 %-løsningen CanalPro hadde høyere pH enn 5 %-løsningen i forsøket. Trolig skyldes det at CanalPro er stabilisert med tilsetting av lut som hever pH-verdien. Dette gjør løsningen tyngre å bufre, noe som påvirker toksisiteten negativt ved at den vil være svært reaktiv hvis uhell skulle oppstå. CanalPro finnes også som en 6 %-løsning.
Zehnder og medarbeidere har også sett på sammenhengen mellom konsentrasjon (0,5 og 2,5 % NaOCl-løsninger) og bufring på vevsoppløselighet av preparater hentet fra ferskt og nekrotisk muskelvev hos gris, men disse var 5 ganger tyngre enn vevspreparatene i vår studie [4]. Resultatene fra ferskt og nekrotisk vev var tilnærmet lik. En 0,5 % ubufret og en 0,5 % bufret løsning (Dakins løsning) viste seg å ha tilnærmet samme vevsoppløsende effekt, hvor vekten etter 60 minutter var redusert med omtrent 50 %. For en ubufret 2,5 %-løsning var gjenværende vevsmasse for ferskt vev omkring 10 %. Sammenlignet med våre resultater tok det lengre tid før preparatene var fullstendig oppløst, noe som nok har sammenheng med størrelsen på vevspreparatene som var benyttet. I likhet med Zehnder sin studie er det grunn til å tro at det er tilgjengelig mengde klor som er den avgjørende faktor for vevsoppløsende evne, og i mindre grad pH.
I motsetning til Zehnder sin studie viste Gordon og medarbeiderne at det var minimale forskjeller mellom NaOCl-løsninger på 1, 3 og 5 % når det gjaldt oppløsning av nekrotisk vev [15]. Dette er et klinisk relevant funn siden mye av den endodontiske behandlingen gjøres i tenner med infisert nekrotisk pulpa. Noe av forklaringen kan ligge i at nedbrytningen av proteinkjedene i nekrotisk infisert vev allerede er begynt. Spesielt er dette interessant for bufrede løsninger som har betydelig bedre antibakteriell effekt(1-6, 16).
Ved blanding med vann vil NaOCl spaltes til NaOH og HOCl [2][5]. Senkning av pH øker mengden tilgjengelig HOCl, siden spaltingen av HOCl til H+og OCl-avtar. Ved nedbrytning av nitrogenbindinger i peptidene frigjøres nitrogen og karbondioksid. Det er nettopp dette vi ser når hypoklorittløsningen kommer i kontakt med preparatene. I kontakt med proteiner vil hypokloritt også danne kloraminer som er viktig for den antibakterielle effekt [3]. Tilgjengelig HOCl øker med bufring og gjør løsningen mer antibakteriell [16].
Siden NaOCl ikke er selektivt oppløsende, vil utilsiktet søl eller utpressing av irrigasjonsveske kunne gi skade på omkringliggende vev [8][9]. I kontakt med vitalt vev vil ubufret NaOCl hurtig oksidere omliggende vev, noe som fører til hemolyse og ulcerasjon, hemming av nøytrofil migrasjon og destruksjon av endotel og fibroblaster [17]. En NaOCl-løsning med konsentrasjoner på opp mot 5 % er sterkt hypertonisk [18]. Til sammenligning har en isoton løsning en saltkonsentrasjon på 0,9 %. Det osmotiske trykket blir derfor svært høyt, og kan resultere i omfattende ødem om uhellet er ute. Et annet forhold som ikke tidligere er beskrevet i særlig grad er sammenheng mellom konsentrasjon og postoperativ smerte. Av tilgjengelig litteratur er det funnet at økt konsentrasjon på NaOCl-løsninger påvirker symptombildet negativt. Sammenligning av en 1,3 % mot en 5,25 % løsning viste en signifikant reduksjon (opptil 60 %) i opplevd postoperativ smerte [19].
Betydning av bufring for vevsoppløsende og antibakteriell effekt
pH i løsningen bestemmer fordelingen av tilgjengelig klor i form av OCl- og HOCl. Høy pH fører til at alt tilgjengelig klor forekommer i form av OCl-. Ved nøytral pH (ca pH 7), vil det meste av tilgjengelig klor være i form av HOCl og fravær av hydroksidioner. De vevsoppløsende egenskapene til NaOCl-løsninger er forbundet med høy konsentrasjon av OCl-, mens den baktericide effekten først og fremst er knyttet til konsentrasjon av HOCl [16][19]. En senkning av pH fra 11,5 til 9,5 vil gi 100 ganger økning av HOCl. Det er derfor en positiv korrelasjon mellom senket pH (bufring) og antibakteriell effekt av NaOCl-løsninger [1][2][3][4][5][6][16]. Høye konsentrasjoner av HOCl virker toksisk på bakterier, ettersom de lett trenger inn i cellen og danner kloraminer med intracellulære proteiner. Dannelse av kloraminer bidrar til den antibakterielle effekten. Hydroksidioner som en finner i ubufrede løsninger med høy pH kan reagere med fettsyrer i vevet i en reaksjon som kalles forsåping. Dette kan gi etseskader og ødem [20]. Også OCl- som er viktig for vevsoppløselighet bidrar med en vevstoksisk effekt. Følgelig ønsker vi at NaOCl-løsningene som brukes skal optimaliserer de antimikrobielle egenskaper som en oppnår med senkning av pH, samtidig som de bevarer tilstrekkelig oppløsende effekt på nekrotisk vev. En bør derfor tilstrebe å benytte løsninger med pH på litt over 9 [5][6][16].
Selektiv toksisitet er et medikament sin evne til å uskadeliggjøre/drepe patogener uten å skade vertens egne celler. Dette er typisk for antibiotikapreparater. Disse kjennetegnes ved at medikamentet angriper biokjemiske prosesser eller bestanddeler som er spesielt for patogenet. NaOCl-løsninger skiller ikke mellom bakterier og kroppens egne celler. Derfor er det viktig å balansere de vevsoppløselige egenskapene opp mot tilstrekkelig antibakteriell effekt.
Oppsummering
Det anbefales det å benytte NaOCl-løsninger som balanserer de vevsoppløselige og antibakterielle egenskapene. Den generelle anbefaling vil være å benytte løsninger som bufres til en pH i området 9,0 - 9,5. Løsningen er da bedre med tanke på antimikrobiell effekt, samtidig som risiko for alvorlige komplikasjoner grunnet vevsoppløselig og toksisk effekt reduseres. I tillegg vil konsentrasjoner omkring 1 % ha tilstrekkelige antibakterielle og vevsoppløsende egenskaper.
Referanser
Kristoffersen Ø, Fristad I. Natriumhypokloritt – anbefalinger og praktisk bruk. Nor Tannlegeforen Tid. 2007; 117: 656–60.
Dakin HD. On the use of certain antiseptic substances in the treatment of infected wounds. Br Med J. 1915; 2: 318-20.
Gustafsson L. Dakins solution; chemistry, preparation, properties and stability. Odontol Tidskr. 1966; 74: 262-73.
Zehnder M, Kosicki D, Luder H, Sener B, Waltimo T. Tissue-dissolving capacity and antibacterial effect of buffered and unbuffered hypochlorite solutions. Oral Surg Oral Med Oral Pathol Oral Radiol Endod. 2002; 94: 756-62.
Christensen CE, McNeal SF, Eleazer P. Effect of lowering the pH of sodium hypochlorite on dissolving tissue in vitro. J Endod. 2008; 34: 449-52.
RELIS Sør. Holdbarhet av natriumhypoklorittløsning etter anbrudd/klargjøring. RELIS - Produsentuavhengig legemiddelinformasjon for helsepersonell. 1999. https://relis.no/sporsmal_og_svar/2-1292?source=relisdb (lest 22.03.2022).
Radcliffe CE, Potouridou L, Qureshi R, Habahbeh N, Qualtrough A, Worthington H, Drucker DB. Antimicrobial activity of varying concentrations of sodium hypochlorite on the endodontic microorganisms Actinomyces israelii, A. naeslundii, Candida albicans and Enterococcus faecalis. Int Endod J. 2004; 37: 438-46.
Hülsmann M, Hahn W. Complications during root canal irrigation--literature review and case reports. Int Endod J. 2000; 33: 186-93.
Regalado Farreras DC, Puente CG, Estrela C. Sodium hypochlorite chemical burn in an endodontist’s eye during canal treatment using operating microscope. J Endod. 2014; 40: 1275-9.
Guerrero-Jiménez M, Nic-Can GI, Castro-Linares N, Aguilar-Ayala FJ, Canul-Chan M, Rojas-Herrera RA, Peñaloza-Cuevas R, Rodas-Junco BA. In vitro histomorphometric comparison of dental pulp tissue in different teeth. PeerJ. 2019; 7: e8212.
Mendez JD, Zarzoza E. Rapid determination of dry weight in human dental pulp by a colorimetric reaction. J Endod. 1999; 25: 596-8.
Sirtes G, Waltimo T, Schaetzle M, Zehnder M. The effects of temperature on sodium hypochlorite short-term stability, pulp dissolution capacity, and antimicrobial efficacy. J Endod. 2005; 31: 669-71.
Abou-Rass M, Oglesby SW. The effects of temperature, concentration, and tissue type on the solvent ability of sodium hypochlorite. J Endod. 1981; 7: 376-7.
Cunningham WT, Joseph SW. Effect of temperature on the bactericidal action of sodium hypochlorite endodontic irrigant. Oral Surg Oral Med Oral Pathol. 1980; 50: 569-71.
Gordon TM, Damato D, Christner P. Solvent effect of various dilutions of sodium hypochlorite on vital and necrotic tissue. J Endod.1981; 7: 466-9.
Johns CK. Germicidal power of sodium hypochlorite. Ind Eng Chem. 1934; 26: 787-8.
Pashley EL, Birdsong NL, Bowman K, Pashley DH. Cytotoxic effects of NaOCl on vital tissue. J Endod .1985; 11: 525-8.
Zhu WC, Gyamfi J, Niu LN, Schoeffel GJ, Liu SY, Santarcangelo F, Khan S, Tay KCY, Pashley DH, Tay FR. Anatomy of sodium hypochlorite accidents involving facial ecchymosis - a review. J Dent. 2013; 41: 935-48.
Mostafa M, El-Shrief YAI, Anous WIO, Hassan MW, Salamah FTA, El Boghdadi RM, El-Bayoumi MAA, Seyam RM, KG Abd-El-Kader KG, Amin SAW. Postoperative pain following endodontic irrigation using 1.3% versus 5.25% sodium hypochlorite in mandibular molars with necrotic pulps: a randomized double-blind clinical trial. Int Endod J. 2020; 53: 154-66.
Jungbluth H, Marending M, De-Deus G, Sener B, Zehnder M. Stabilizing sodium hypochlorite at high pH: effects on soft tissue and dentin. J Endod. 2011; 37: 693-6.
English summary
Myklebust PED, Fossgård M, Fristad I.
Sodium hypochlorite and tissue-dissolving properties
Nor Tannlegeforen Tid. 2022; 132: 838-42.
The purpose of this study was to study tissue-dissolving properties and pH of various commercially available sodium hypochlorite solutions. Tissue solubility of the sodium hypochlorite solutions, both in buffered and unbuffered form, was studied using tissue samples from muscle tissue in pigs. All available sodium hypochlorite solutions were unbuffered. The tissue dissolving properties were more dependent on concentration than on pH, although the clinical relevance may be discussed. In clinical practice, it is important to balance the tissue-dissolving effect against toxicity and antibacterial properties. The manufacturers of commercially available sodium hypochlorite solutions appear to solely focus on shelf-life rather than toxicity and antibacterial properties.
Korresponderende forfatter: Inge Fristad, e-post: inge.fristad@uib.no
Akseptert for publisering18.08.2022
Artikkelen er fagfellevurdert
Myklebust PED, Fossgård M, Fristad I. Natriumhypokloritt og vevsoppløselighet. Nor Tannlegeforen Tid. 2022; 132: 838-42.
Norsk MeSH: Endodonti; Natriumhypokloritt; Kjemisk virkning og bruk
Studien bygger på en prosjekt-/masteroppgave i odontologistudiet studiet ved UiB.
