Botulinumtoksin - en oversikt over mulige bruksområder innen oral og maxillofacial kirurgi
cand.odont., spesialistkandidat og assistenttannlege. Avdeling for oral kirurgi og oral medisin, Institutt for klinisk odontologi, Universitetet i Oslo og Avdeling for kjevekirurgi og sykehusodontologi, Oslo universitetssykehus HF - Rikshospitalet
dr.med., professor og avdelingsoverlege. Avdeling for kjevekirurgi og sykehusodontologi, Oslo universitetssykehus HF - Ullevål
cand.odont., universitetslektor og PhD-stipendiat. Avdeling for oral kirurgi og oral medisin, Institutt for klinisk odontologi, Universitetet i Oslo
Botulinumtoksin er et neurotoksin produsert av bakterien Clostridium botulinum, og blir i raffinert form brukt til ulike typer medisinsk behandling. De fleste er i dag kjent med bruken av botulinumtoksiner innen kosmetisk medisin for å behandle ansiktsrynker. Botox® (Allergan Inc, USA) og Dysport® (Ipsen Biopharm Ltd, UK) er to eksempler på botulinumtoksiner som anvendes i kosmetisk medisin og dermatologi. I de senere årene har man rapportert om flere ulike bruksområder for botulinumtoksiner også innenfor oral og maxillofacial kirurgi, blant annet for pasienter med muskelspasmer, hypersalivasjon, hypertrofisk kjevemuskulatur og kjeveleddsplager. Internasjonalt kan man også se en antydning til bruk av botulinumtoksiner innen generell odontologi. Botulinumtoksiner har potensielt mange bruksområder, også innenfor oral- og maxillofacialkirurgisk spesialistbehandling. Bruk av botulinumtoksiner synes å være en behandlingsmetode med lovende resultater, men man har per i dag ikke et godt nok vitenskapelig grunnlag for å kunne anse dette som annet enn eksperimentell behandling. Forfatterne støtter ikke bruk av botulinumtoksiner i generell odontologisk praksis og anser flere av de beskrevne prosedyrene som institusjonsbehandling på spesialistnivå. Det er likevel viktig for tannleger å kjenne til behandlingsmulighetene botulinumtoksiner gir innenfor det orofaciale området.
Forgifting med botulinumtoksin (BTX), kalt botulisme, er en livstruende sykdom. Hovedsymptomene er kvalme, oppkast, synsforstyrrelser og pareser, og man dør som regel av respirasjonssvikt. Toksinene kan finnes i næringsmidler som spises uten å først bli varmebehandlet, blant annet rakfisk, hjemmelaget spekeskinke og hjemmehermetiserte kjøttvarer. Toksinene produseres under bakterieveksten og akkumuleres i næringsmiddelet. Senter for mattrygghet ved Norges Veterinærhøgskole opplyser følgende (1):
«Botulisme er en sjelden sykdom både i Norge og resten av verden. Fra 1957 er det rakfisk som har dominert botulismebildet i Norge. Fra 1977 - 2005 er det meldt om 45 tilfeller med kun ett dødsfall (matbåren). Av disse er 6 sårbotulisme, og 4 tilfeller av spedbarnsbotulisme forårsaket av importert kontaminert honning».
De første rapporterte tilfellene av botulisme ble gjort av den tyske legen og poeten Justinus Kerner (1786 - 1862), som kalte det «pølseforgiftning». Han så at inntak av kjøtt- og blodpølser førte til dødsfall hos mange mennesker, og han beskrev symptomene til matbåren botulisme. Han fremmet også teorien om at BTX kunne brukes til terapeutiske formål. «Botulus» betyr pølse på latinsk (2). Emile van Ermengem isolerte i 1897 Clostridium botulinum-bakterien fra skinke og brukte denne til å fremstille BTX som han injiserte i forsøksdyr og fremkalte botulisme (3). BTX ble på 1900-tallet utviklet til bruk i biologisk krigføring, men i de fleste land stoppet man dette og fortsatte kun foredlingen av BTX til medisinsk bruk. I 1972 studerte Scott og medarbeidere effekten av botulinumtoksin type A i primater, og mot slutten av 70-tallet ble bruk av toksinet fremmet som en behandlingsform for strabismus (skjeling) (4). Ikke før mot slutten av 80-tallet rapporterte man om bruk av BTX i behandling av ansiktsrynker, og utover 90-tallet ble bruken mer populær og bruksområdet stadig utvidet (figur 1) (5).
Figur 1. Eksempel på mye kommersielt brukt botulinumtoksin type A. Gjengitt med tillatelse fra Allergan Norden AB, Upplands Väsby, Sverige.
Virkningsmekanisme
Clostridium botulinum er en Gram-positiv, anaerob, sporedannedende bakterie, som finnes i jord og marine sedimenter over hele verden (6). Det er beskrevet sju ulike clostridium-arter (A, B, C (1 og 2), D, E, F og G), som hver produserer sitt distinkte neurotoksin som navngis etter respektive bakterieart (BT-A, -B, -C, -D, -E, -F, -G). De sju neurotoksinene er strukturelt sett ganske like, men immunologisk forskjellige. Det er normalt sett bare BT-A, -B, -E, -F og -G som affiserer mennesker (7).
Botulinumtoksinet er det mest toksiske materialet som er kjent. Til eksempel er det 4 ganger mer dødelig i mus enn tetanustoksinet, 1 x 1010 mer dødelig enn curare og 100 x 1010 mer dødelig enn natriumcyanid (8). Dødelig dose for et menneske på 70 kg anslås til å være 0,09 - 0,15 mg ved intravenøs administrasjon, 0,7 - 0,9 mg ved inhalasjon og 70 mg ved oral administrasjon (9).
Botulinumtoksin type A (BTX-A) er den mest anvendte til terapeutiske formål. Den virker ved å hemme utskillelsen av acetylkolin (AK) i kontaktflaten mellom nerve ende og muskelcelle. Normalt sett vil utskillelse av acetylkolin medføre at disse bindes til AK-reseptorer på den motoriserte endeplaten av muskelcellen, og dette fører til at natrium- og kaliumkanaler åpnes. Dette initierer depolarisering av endeplaten og til slutt kontraksjon av muskelcellen. BTX-A inhiberer utskillelsen av AK og hemmer dermed muskelkontraksjonen (figur 2). Denne inhibisjonen er temporær, da det over tid foregår en knoppskyting av nye nerveender og redanning av nerve-muskel synapser slik at man reetablerer neuromuskulær transmisjon (10). Forskning antyder at BTX-A også bidrar til å redusere frigivelsen av inflammasjonsmediatorer som medfører smerte, blant annet kalsitonin genrelatert peptid (CGRP), substans P og glutamat (11).
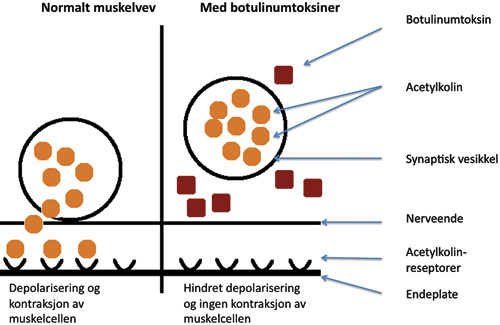
Figur 2. Forenklet illustrasjon av virkningsmekanismen til botulinumtoksin på muskelceller.
Ved bruk i klinikken ser man begynnende effekt av injeksjon med BTX-A etter 1 - 7 dager, og deretter 1 - 2 uker med maksimal effekt. Effekten stabiliserer seg i en periode og avtar så gradvis samtidig som man har en gradvis reetablering av innervasjonen. Etter 3 - 6 måneder har man som regel gjenvunnet full nerveinnervasjon av den aktuelle muskel (12).
Behandlingsformer
Innen kosmetisk kirurgi og kosmetisk medisin er bruk av BTX mest forbundet med utjevning av rynkete ansiktshud. I denne oversikten fokuseres det på mulige bruksområder av BTX innen oral og maxillofacial kirurgi: habituell kjeveleddsluksasjon, hypertrofi av m. masseter og m. temporalis, spyttsekresjonsforstyrrelser, temporomandibulær dysfunksjon, ansiktssmerter, neuromuskulære forstyrrelser og facialisparese.
Habituell kjeveleddsluksasjon
Luksasjon av kjeveleddet defineres som en fullstendig utglidning av leddhodet fra leddskålen, og leddhodet låses foran eminensen (13). Tilstanden klassifiseres normalt som akutt, tilbakevendende eller habituell. Den akutte tilstanden er relativt vanlig og kan oppstå etter traume, spontant eller på grunn av psykisk sykdom. Når luksasjonen oppleves oftere, samt utvikler seg til å bli verre og plagsom for pasienten, omtales den gjerne som tilbakevendende eller habituell og i langvarige tilfeller som kronisk. Behandlingen av habituell kjeveleddsluksasjon går ut på å injisere BTX-A i m. pterygoideus lateralis, og dermed lamme en av musklene som er med på å trekke leddhodet frem over eminensen. Man stikker perkutant i området under arcus zygomaticus og mellom processus coronoideus og collum. Innstikket må være 3 - 4 cm for å nå inn til muskelen, og behandlingen har effekt i omtrent 3 måneder. Fu og medarbeidere fulgte fem pasienter med nevrologisk og eller systemisk sykdom, og Bouso og medarbeidere rapporterte om 4 pasienter med nevrologisk sykdom der injeksjon med BTX-A ble ansett som suksessfull behandling (14, 15). Injeksjonsterapi kan være et konservativt og reversibelt alternativ til kirurgi (figur 3).
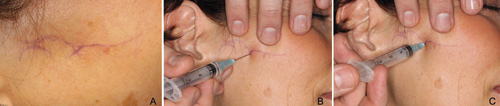
Figur 3. Demonstrasjon av injeksjon i m. pterygoideus lateralis dexter. Forfatterne oppfordrer til bruk av hansker i reelle behandlingssituasjoner. Fotos: H. Øyri.
Hypertrofi av m. masseter og m. temporalis
Hypertrofi av m. masseter (uni- og bilateralt) kan skyldes habituelle forhold, som asymmetrisk bruk av kjevemuskulatur og bruxisme, eller kongenitale malformasjoner. Kirurgisk korreksjon er et behandlingsalternativ for disse pasientene. Intramuskulære injeksjoner med BTX-A i m. masseter har i kliniske studier vist god effekt ved muskelhypertrofi, og vil kunne være et godt behandlingsalternativ til kirurgisk korreksjon. Det antydes likevel at man trenger randomiserte kontrollerte studier for å understøtte denne behandlingsformen (16). Forekomsten av muskelhypertrofi i m. temporalis er sjeldnere, men det rapporteres om godt resultat etter behandling med intramuskulær injeksjon med BTX-A uten nevneverdige bivirkninger (17).
Spyttsekresjonsforstyrrelser
Ved ulike former for neurologisk sykdom kan pasientene ha en kraftig hypersalivasjon, sialorrhoea, og være plaget med sikling. Injeksjoner med BTX-A har i mange år vært benyttet som behandling for sialorrhoea hos pasienter med Parkinsons sykdom, amytropisk lateral sklerose og cerebral parese, og man har fått god effekt og få komplikasjoner (18). Noen forfattere stiller imidlertid spørsmål ved dette (19).
Man har også benyttet BTX-A i behandlingen av sialoceler og fistler etter sialoadenektomi, cancerkirurgi i orofarynx, eller ved inngrep som krever tilgang gjennom parotis (20). Videre rapporterer man også om god effekt hos pasienter med Frey''s syndrom og pasienter med tilbakevendende eller kronisk parotitt (21). Frey''s syndrom, også omtalt som «gustatorisk svette», er et sjeldent sekvele som kan oppstå etter blant annet parotiskirurgi. Det kjennetegnes ved at det ved smaksstimulering oppstår svette og rødme i et område over, foran og under øret. I de fleste tilfeller der BTX brukes til behandling av spyttsekresjonsforstyrrelser, fokuseres det hovedsakelig på gl. parotis og i mindre grad på gl. submandibularis. Gl. sublingvalis blir sjelden injisert. Injeksjonene gis intraparenkymalt eller rundt kjertelen, og noen forfattere benytter seg av elektromyografiske (EMG) - eller ultralydguidete injeksjoner.
Temporomandibulær dysfunksjon
Temporomandibulær dysfunksjon, TMD, er en samlebetegnelse på en rekke tilstander i kjevemuskulatur, kjeveledd og tilgrensende strukturer. Hos pasienter med trismus, eller annen form for begrenset munnåpning, har de fleste opplevd noe øket gapehøyde etter behandling (22). Intramuskulære injeksjoner med BTX samtidig med arthrocentese av kjeveleddet har vist oppløftende resultater i forhold til forlenget effekt av behandlingen, og det er foreslått at det muligens kan være en synergistisk effekt av de to prosedyrene (23). Klikking fra kjeveleddet som følge av anterior diskusdisplassering har også blitt behandlet med BTX med gode resultater (24). Det er dog omdiskutert hvorvidt dette er en tilstand som skal behandles.
Ansiktssmerter
Studier har vist effekt av BTX-A i behandlingen av kroniske smertetilstander som for eksempel tensjonshodepine, myofascial smerte, migrene og trigeminusnevralgi (25). Man har også sett positive resultater ved behandling av sårsmerte etter rekonstruktiv kjeve- og ansiktskirurgi, konvensjonell og endoskopisk bihulekirurgi og kjeveleddskirurgi. Yoon et al. rapporterer om ett tilfelle med mulig effekt av subkutan injeksjon med BTX-A i behandlingen av neuropatiske smerter etter skade på n. alveolaris inferior (26). Det finnes ingen sammenlikningsstudier som vurderer bruken av BTX i forhold til konvensjonell smertebehandling.
«Tics»/dystonier - neuromuskulære forstyrrelser
Lokal behandling av dystoni (ukontrollerbare kontraksjoner av spesifikke muskler) og muskelspasmer har lenge blitt håndtert med BTX-injeksjoner. BTX-A og BTX-B har vist jevngode resultater, og det regnes som en trygg og forutsigbar behandling (27, 28). I litteraturen nevnes blant annet disse neuromuskulære forstyrrelsene: oromandibulær dystoni (29), cervikal dystoni (30), hemifaciale spasmer (31), tardive (langsomme) dyskinesier (32), tardive tungeprotrusjons dystonier (33) og hyperkinetiske forstyrrelser i platysma (34).
Facialisparese
De fleste pasienter som rammes av facialisparese har etter 3 - 5 måneder gjenvunnet normal ansiktsmimikk. Et fåtall har sekveler av ulik alvorlighetsgrad og de kan ha et ansikt med skjemmende asymmetriske forandringer (35). BTX-A kan hos noen brukes på den friske siden for å utjevne forskjeller og på denne måten bidra til å kamuflere asymmetrier. Andre pasienter er plaget av synkinese, som beskrives som ufrivillige og ukoordinerte muskelkontraksjoner assosiert med frivillige muskelkontraksjoner. Hos denne pasientgruppen kan BTX-A brukes til å dempe symptomene (36). Videre kan injeksjoner med BTX-A i m. levator palpebrae superioris benyttes til å indusere ptose (nedsunket øyelokk) og dermed bidra til å forhindre uttørking av hornhinnen (37).
Komplikasjoner
Bruken av BTX innen ulike medisinske prosedyrer anses å være en trygg behandlingsform med få komplikasjoner og bivirkninger, under forutsetning av at behandler er trent. Det rapporteres sjelden om systemiske bivirkninger, men dette kan omfatte forbigående muskelsvakhet, trøtthet, kvalme, kløe og influensaliknende symptomer. Behandlingsresistens mot BTX-A anslås å være rundt 7 %, og man undersøker om BTX-B kan være et alternativ for disse pasientene. Pasienter som har fått BTX-injeksjoner flere ganger tidligere, kan utvikle sekundærresistens som følge av produksjon av nøytraliserende antistoffer (38). I fremstillingen av ulike typer BTX-A brukes albumin derivert fra humant blod, og dette medfører både en fare for allergiske reaksjoner og en teoretisk mulighet for smittefare (39). Lokale komplikasjoner rundt injeksjonsstedet og i omkringliggende vev anses å være de vanligste bivirkningene ved bruk av BTX-A. Mild smerte, erytem, ekkymoser og lett hevelse i injeksjonsområdet er relativt vanlig. Videre rapporteres det om tørre øyne, hengende munnvik, ptose og ødem i øvre øyelokk, svakhet i ansiktsmuskler, assymetriske ansiktsuttrykk, xerostomi, forbigående dysfagi, begrenset munnåpning, lekkasje til nesen ved matinntak, nasal stemme, hodepine, uklart syn, løs mage, problemer med å tygge, engstelse for aspirasjon ved pusting, kjeveleddssubluksasjoner, taleproblemer, spyttsten, lokale skader på carotisarterier og grener av n. facialis (40). Xerostomi og dysfagi sees oftere etter behandling med BTX-B enn ved bruk av BTX-A (41).
Kontraindikasjoner
I litteraturen rapporterer man om få kontraindikasjoner ved behandling med BTX-A. Produsenten av Botox® (Allergan Inc, USA), en mye brukt type BTX-A, har oppført en rekke potensielle kontraindikasjoner i sitt pakningsvedlegg. Dette omfatter blant annet personer som er gravide eller ammende, personer med neuromuskulær sykdom, f.eks. myasthenia gravis, amyotrofisk lateralsklerose, Eaton-Lambert syndrom (autoimmun sykdom med muskelsvakhet i ekstremitetene) og myopatier), mulige legemiddelinteraksjoner (aminoglykoside antibiotika, quinidine, Ca2+-blokkere, magnesiumsulfat, suksametonium og polymyxin) og personer som er allergiske mot ett eller flere av virkestoffene. Videre frarådes det å injisere i vev med inflammasjonstegn (42).
Oppsummering
Publisert litteratur vedrørende bruk av BTX innen oral og maxillofacial kirurgi preges av kasuistikker, pilotstudier og andre små studier med lav grad av evidens. Det fremholdes, både av produsenter og flere forfattere, at kommersielt tilgjengelige BTX i dag er enkle å håndtere, de aksepteres bra av de fleste pasienter og de har svært få bivirkninger. Man kan med dette kunne oppfordre til økt bruk av disse preparatene på tvilsomme indikasjoner, samt øke bruken blant operatører uten adekvat opplæring og kompetanse. Kontraindikasjoner og potensielle skadevirkninger etter kort- og langtidsbruk bør sannsynligvis heller ikke bagatelliseres. Man mangler større studier der konvensjonelle, etablerte behandlingsmetoder sammenliknes med BTX. Studier med lang oppfølgingstid vil også kunne bidra til å avdekke eventuelle langtidseffekter og bivirkninger.
Botulinumtoksiner har potensielt mange ulike bruksområder, også innenfor oral- og maxillofacialkirurgisk spesialistbehandling. Det virker som en behandlingsmetode med lovende resultater, men man har per i dag ikke et godt nok vitenskapelig grunnlag for å kunne anse dette som annet enn eksperimentell behandling sammenliknet med etablerte og mer veldokumenterte behandlingsmetoder. Forfatterne støtter ikke bruk av botulinumtoksiner i generell odontologisk praksis og anser flere av de beskrevne prosedyrene som institusjonsbehandling på spesialistnivå.
Hovedbudskap | |
|---|---|
· |
Botulinumtoksin er et neurotoksin produsert av bakterien Clostridium botulinum |
· |
Innenfor oral og maxillofacial kirurgi kan botulinumtoksiner blant annet brukes hos pasienter med muskelspasmer, hypersalivasjon, hypertrofisk kjevemuskulatur og kjeveleddsplager |
· |
Man har manglende vitenskapelig grunnlag for å underbygge flere av de aktuelle indikasjonsområdene og behandlingsmetodene |
· |
Forfatterne støtter ikke bruk av botulinumstoksiner i generell odontologisk praksis og anser flere av de beskrevne prosedyrene som institusjonsbehandling på spesialistnivå |
English summary
Øyri H, Skjelbred P, Olsen-Bergem H.
Potential clinical use of botulinum toxin in oral and maxillofacial surgery
516 - 20.
Botulinum toxin is a neurotoxin produced by the bacterium Clostridium botulinum, and is in refined form used for different types of medical treatment. Most people are familiar with the use of botulinum toxins in cosmetic medicine to treat facial wrinkles. Over recent years there have been reports of several different uses for botulinum toxins in oral and maxillofacial surgery, including for patients with muscle spasms, sialorrhea, hypertrophic facial muscles, and TMD. Internationally there seems to be a growing interest in and use of botulinum toxins in general dentistry. Botulinum toxins potentially have many different applications, including in the field of specialist care provided by oral and maxillofacial surgeons. The use of botulinum toxins in oral and maxillofacial surgery is shows promising results, but there is not enough scientific evidence to consider it to be anything but an alternative treatment compared to established and more proven therapy. The authors do not support the use of botulinum toxins in general dental practice and consider the described procedures as specialist care.
Forfatterne angir ingen interessebindinger.
Referanser
Norges veterinærhøgskole. Clostridium botulinum http://www.veths.no/PageFiles/691/C %20botulinum %20Senteret.pdf (lest 30.03.12)
Erbguth FJ. From poison to remedy: the chequered history of botulinum toxin. J Neural Transm. 2008; 115: 559 - 65.
Cherington M. Botulism: update and review. Semin Neurol. 2004; 24: 155 - 63.
Scott AB. Botulinum toxin injections in eye muscles to correct strabismus. Trans Am Ophthalmol Sec. 1981; 79: 734 - 70.
Niamtu J. Aesthetic uses of botulinum toxin A. J Oral Maxillofac Surg. 1999: 57: 1228 - 33.
Sugiyama H. Clostridium botulinum neurotoxin. Microbiol Rev. 1980: 44: 419 - 448.
Huang W, Foster JA, Rogachefsky AS. Pharmacology of botulinum toxin. J Am Acad Dermatol. 2000; 43: 249 - 59.
Carruthers A, Carruthers J. Botulinum toxin type A: History and current cosmetic use in the upper face. Semin Cutan Med Surg. 2001; 20: 71 - 84.
Arnon SS. Botulinum toxin as a biological weapon. JAMA. 2001: 285: 1059 - 1070.
Blitzer A, Sulica L. Botulinum toxin: basic science and clinical uses in otolaryngology. Laryngoscope. 2001; 111: 218 - 26.
Song PC, Schwartz J, Blitzer A. The emerging role of botulinum toxin in the treatment of temporomandibular disorders. Oral Diseases. 2007: 13: 253 - 60.
Sadick NS, Matarasso SL. Comparison of botulinum toxins A and B in the treatment og facial rhytides. Dermatol Clin. 2004; 22: 221 - 6.
Undt G, Kermer C, Piehslinger E, Rasse M. Treatment of recurrent mandibular dislocation. Part I. Leclerc blocking procedure. Int J Oral Maxillofac Surg. 1997; 26: 92 - 7.
Fu K-Y, Chen H-M, Sun Z-P, Zhang Z-K, Ma X-C. Long-term efficacy of botulinumtoxin type A for the treatment of habitual dislocation of the temporomandibular joint. Br J Oral Maxillofac Surg. 2010; 48: 281 - 4.
Bouso OV, González GF, Mommsen J, Grau VG, Fernández JR, Micas MM. Neurogenic temporomandibular joint dislocation treated with botulinum toxin: report of 4 cases. Oral Surg Oral Med Oral Pathol Oral Radiol Endod. 2010; 109: e33 - 7.
Al-Muharraqi MA, Fedorowicz Z, Al Bareeq J, Al Bareeq R, Nasser M. Botulinum toxin for masseter hypertrophy. Cochrane Database Syst Rev. 2009; 21: CD007510. Review.
Isaac AM. Unilateral temporalis muscle hypertrophy managed with botulinum toxin type A. Br J Oral Maxillofac Surg. 2000; 38: 571 - 2.
Porta M, Gamba M, Bertacci G. Treatment of sialorrhea with ultrasound guided botulinum toxin type A injection in patients with neurological disorders. J Neurol Neurosurg Psychiatry. 2001; 70: 538 - 40.
Nordgården H, Østerhus I, Møystad A, Asten P, Johnsen UL, Storhaug K, Loven JO. Drooling: Are Botulinum toxin injections into the major salivary glands a good treatment option? J Child Neurol. 2012; 27: 458 - 64.
Marchese-Ragona R, Marioni G, Restivo AD. The role og botulinum toxin in postparotidectomy fistula treatment. A technical note. Am J Otolaryngol. 2006; 27: 221 - 4.
Capaccio P, Torretta S, Osio M, Minorati D. Botulinum toxin therapy: a tempting tool in the management of salivary secretory disorders. Am J Otolaryngol. 2008: 29: 333 - 338.
Freund B, Schwartz M, Symington JM. Botulinum toxin: new treatment for temporomandibular disorders. Br J Oral Maxillofac Surg. 2000; 38: 466 - 71.
Freund BJ, Schwartz M. Intramuscular injection of botulinum toxin as an adjunct to arthrocentesis of the temporomandibular joint: preliminary observations. Br J Oral Maxillofac Surg. 2003; 41: 351 - 2.
Bakke M, Møller E, Werdelin LM, Dalager T, Kitai N, Kreiborg S. Treatment of severe temporomandibular joint clicking with botulinum toxin in the lateral pterygoid muscle in two cases of anterior disc displacement. Oral Surg Oral Med Oral Pathol Oral Radiol Endod. 2005; 100: 693 - 700.
Borodic GE, Acquadro MA. The use of botulinum toxin for the treatment of chronic facial pain. J Pain. 2002; 3: 21 - 7.
Yoon SH, Merrill RL, Choi JH, Kim ST. Use of botulinum toxin type A injection for neuropathic pain after trigeminal nerve injury. Case Report. Pain Medicine. 2010; 11: 630 - 2.
Jankovic J, Orman J. Botulinum A toxin for cranial-cervikal dystonia: a double-blind, placebo-controlled study. Neurology. 1987; 37: 616 - 623.
Comella CL, Jankovic J, Shannon KM, Tsui J, Swenson M, Leurgans S, Fan W. Comparison of botulinum toxin seroptypes A and B for the treatment of cervical dystonica. Neurology. 2005; 65: 1423 - 1429.
Tan EK, Jankovic J. Botulinum toxin A in patients with oromandibular dystonia: long-term follow-up. Neurology. 1999; 53: 2102 - 7.
Quagliato EM, Carelli EF, Viana MA. A prospective, randomized, double-blind study comparing the efficacy and safety of type a botulinum toxins botox and prosigne in the treatment of cervical dystonia. Clin Neuropharmacol. 2010; 33: 22 - 6.
Yoshimura DM, Aminoff MJ, Tami TA, Scott AB. Treatment of hemifacial spasm with botulinum toxin. Muscle Nerve. 1992; 15: 1045 - 9.
Yasufuku-Takano J, Sakurai M, Kanazawa I, Nagaoka M. Successful treatment of intractable tardive dyskinesia with botulinum toxin. J Neurol Neurosurg Psychiatry. 1995; 58: 511 - 2.
Charles PD, Davis TL, Shannon KM, Hook MA, Warner JS. Tounge protrusion dystonia: treatment with botulinum toxin. South Med J. 1997; 90: 522 - 5.
Laskawi R, Rohrbach S, Rödel R. Surgical and nonsurgical treatment options in patients with movement disorders of the platysma. J Oral Maxillofac Surg. 2002; 60: 157 - 62.
Peitersen E. Bell''s palsy: the spontaneous course of 2,500 peripheral nerve palsies of different etiologies. Acta Otolaryngol. Suppl. 2002; 4: 4 - 30.
Borodic GE, Pearce LB, Cheney M. Botulinum A toxin for treatment of aberrant facial nerve regeneration. Plast Reconstr Surg. 1993; 91: 1042 - 5.
Naik MN, Gangopadhyay N, Fernandes M, Murthy R, Honavar SG. Anterior chemodenervation of levator palpebrae superioris with botulinum toxin type-A (Botox) to induce temporary ptosis for corneal protection. Eye (Lond.) 2008; 22: 1132 - 6.
Göschel H, Wohlfarth K, Frevert J, Dengler R, Bigalke H. Botulinum A toxin therapy: Neutralizing and non-neutralizing antibodies and therapeutic consequences. Exp Neurol. 1997; 147: 96 - 102.
Niamtu J. Botulinum toxin A: A review of 1,085 oral and maxillofacial treatments. J Oral Maxillofac Surg. 2003: 61: 317 - 24.
Majid OW. Clinical use of botulinum toxins in oral and maxillofacial surgery. Int J Oral Maxillofac Surg. 2010; 39: 197 - 207.
Brashear A, Lew MF, Dykstra DD, Comella CL, Factor SA, Rodnitzky RL, Trosch R, Singer C, Brin MF, Murray JJ, Wallace, JD, Willmer-Hulme A, Koller M. Safety and efficacy of NeuroBloc (botulinum toxin type B) in type A-responsive cervikal dystonia. Neurology. 1999; 53: 1439 - 46.
Allergan Pharmaceuticals Ireland. BOTOX® Cosmetic. (onabotulinumtoxinA) for injection. http://www.allergan.com/assets/pdf/botox_cosmetic_pi.pdf (lest 30.03.12)
Adresse: Hauk Øyri, Avdeling for oral kirurgi og oral medisin, Institutt for klinisk odontologi, Universitetet i Oslo, postboks 1109 Blindern, 0317 Oslo. E-post: hauk.oyri@odont.uio.no
Artikkelen har gjennomgått ekstern faglig vurdering.
Øyri H, Skjelbred P, Olsen-Bergem H. Botulinumtoksin - en oversikt over mulige bruksområder innen oral og maxillofacial kirurgi. Nor Tannlegeforen Tid. 2012; 122: 516-20.