Tinnfluorid – en ny fluorforbindelse i Norge
Forfatter
Tinnfluorid har effekt både mot karies og gingivitt, og reduserer også løseligheten av emalje i syre. Tinnfluorid har vært brukt i lang tid av millioner av individer og kan anvendes trygt, og er indisert på individer som har vanskeligheter med å opprettholde en god nok munnhygiene. Tinnfluorid vil også ha effekt mot erosjoner ved å redusere løseligheten av emalje.
Selv om det har vært forskningsmessig interesse for tinnfluorid i Norge, så er det natriummonofluorofosfat (MFP) og senere natriumfluorid som har vært fluorforbindelsene som har vært brukt i tannpasta og skyllevann gjennom de siste 30 – 40 år. Mens USA tok fluortannpasta i bruk i 1950-årene (og vannfluoridering 10 år tidligere), tok det oss ytterligere 20 år å få tilsvarende produkter i praktisk bruk i Norge. Til tross for at vi hadde en meget høy kariesfrekvens, var vi likevel en av de siste landene i Vest-Europa til å benytte oss av det tryllemiddel som fluor i virkeligheten er.
I USA var det tinnfluoridtannpasta som i mange år utgjorde tyngdepunktet i den individuelle kariesprofylakse. Hva er det som er spesielt for tinnfluorid sammenlignet med de andre fluorforbindelsene? Både når det gjelder MFP og NaF, er det fluoridet som har effekt. Natrium og fosfat er bare bærere av fluor; de har ingen klinisk effekt i seg selv. Når det gjelder tinnfluorid derimot, har både tinn og fluor veldokumentert klinisk effekt. Tinnet gir antibakteriell effekt, mens fluoret har effekt mot karies, og er også involvert i tinnfluoridets velkjente løseligreduserende effekt på tannemalje (1).
Tinnfluoridets kjemiske egenskaper
Tinnfluorid er lett løselig i vann og dissosieres i en tinndel (Sn++) og en fluordel (F-). Men det skjer mye mer. Tinnet hydrolyseres: Sn++ + 2H2O Æ Sn(OH)2 + 2H+ (tinnionene danner hydroksid ved å ta opp OH- grupper fra vann, slik at det blir overskudd av H+, løsningen blir sur). Når løsningen når pH 3, skjer følgende reaksjon med fluoret: F- + H20 Æ HF + OH- (fluoret hydrolyseres). Denne reaksjonen gjør at løsningen blir bufret mellom pH 3 og pH 4. Videre reaksjoner mellom tinn og hydroksid stopper på grunn av denne bufringen. Vi har nå en løsning med pH 3 som inneholder tinnioner (Sn++) og fluor (som F- og HF). Denne løsningen har antibakterielle egenskaper på grunn av tinnionene (Sn++) og karieshemmende aktiviteter på grunn av tilstedeværelsen av F- og HF. Det er velkjent at fluor ved lavt pH kan ha bedre kariesforebyggende effekt enn nøytrale fluorløsninger (2).
Hvis et tannsett eksponeres for en løsning av tinnfluorid vil følgende skje: Fluorioner vil danne kalsiumfluorid sammen med kalsium fra tannoverflaten. Dette felles ut på tannemaljen. Samtidig felles det ut et tinnfosfat på de samme tannoverflater ved at tinnioner fra løsningen reagerer med fosfat på tannoverflaten. Disse to reaksjonene bevirker at tannoverflatene raskt blir dekket med en tinn-/fluorfase som gir kariesbeskyttelse. Det er viktig å vite at kariesbeskyttelsen er knyttet til tilstedeværelse av fluorid, og ikke til tinn. Tinnioner uten fluorid, danner et tinnfosfatsjikt, men dette gir ikke kariesbeskyttelse. Det som er anført ovenfor gjelder vandige løsninger av tinnfluorid. I slike løsninger vil det felles ut Sn(OH)2 etter noen dager, og slike løsninger har begrenset holdbarhet (opptil to uker).
Reaksjonene som skjer i en tinnfluoridtannpasta vil være de samme som i løsninger, men mer kompliserte, fordi tannpasta inneholder substanser som kan reagere med både tinn og fluorid. En tannpasta med tinnfluorid vil derfor ofte inneholde en ekstra tinnkilde (tinnpyrofosfat), som avgir tinn etter hvert som den opprinnelige tinnmengden reduseres. Slik tannpasta vil også inneholde stabilisatorer som skal hindre hydrolyse og oksidasjon av tinn. Oksidasjon av tinn (Sn++ Æ Sn++++) gjør at tinnet mister sin antibakterielle aktivitet. Tilsetning av kelatorer (som for eksempel citrat) vil binde Sn++, og dermed hindre oksidasjon (3).
Hva skyldes tinnets antibakterielle egenskaper?
Det er velkjent at en rekke metaller har høy affinitet for svovel og danner sulfider med lav løselighet. Eksempler er ioner av kvikksølv, kobber, bly, sølv, tinn, kadmium og sink. Det er likeledes kjent at svovelholdige aminosyrer (cystein, cystin og methionin) og peptider (f.eks. glutathion) har meget viktige biologiske funksjoner knyttet til thiol(-SH)-grupper. En oksidasjon av en (thiol) gruppe vil ofte inaktivere enzymer. Det er velkjent at glykolysen i bakterier har enzymer som inaktiveres av f.eks. tinn (Fig. 1) (4 – 6).
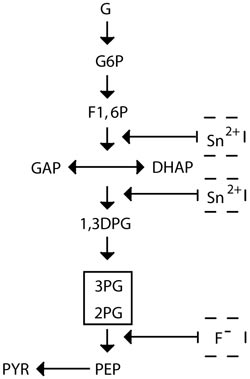
Fig. 1. Figuren viser glykolysen (den trinnvise enzymatiske nedbrytning av glukose til syre). Sn viser steder der tinn inhiberer glykolysen. Tinn og fluor sammen reduserer syreproduksjonen i plakk i lang tid.
Kliniske konsekvenser av tinnets antibakterielle effekt i tinnfluorid
Den mest nærliggende effekt er inhiberingen av plakkdannelse på tenner (7, 8). Det kan sees av illustrasjonen (Fig. 2), at plakkinhiberingen er vesentlig, og at denne tinneffekten hjelper pasientene til å bedre hygienen (9).
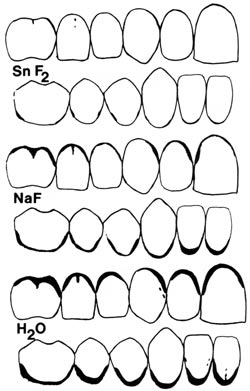
Fig. 2. Figuren er basert på kliniske fotografier der plakk er farget, for å være tydelig. Det kan sees at tinnfluorid har en markert plakkinhiberende effekt (9).
Det er imidlertid ikke bare kvantitativ plakkinhibering som foregår, men også en kvalitativ inhibering. Det er velkjent at tinnfluorid reduserer mengden av streptococcus mutans selektivt i saliva (10). Det er også velkjent at tinnfluorid reduserer frekvensen av «trenchmouth» (ANUG) i militære populasjoner under feltforhold, og at syreproduksjon i plakk reduseres i to-tre timer etter en eksponering for tinnfluorid. Disse effektene ble observert allerede i 1950-årene (11), men det tok lang tid før en forklaring på fenomenene var på plass (5).
En annen konsekvens av tilstedeværelse av Sn++ i munnhulen er en eliminering av dårlig ånde (halitosis) (12). Halitosis skyldes bakteriell dannelse av flyktige, illeluktende, svovelholdige stoffer i munnhulen. Det er hydrogensulfid og metyl merkaptan som er de viktigste gassene, og disse oppstår ved at proteolytiske, anaerobe bakterier bryter ned de svovelholdige aminosyrer cystein og methionin, til de nevnte gasser. Tinn har høy affinitet for svovel og vil stoppe gassdannelsen ved å danne uløselige sulfider med substratene.
Har tinnet andre egenskaper?
Som nevnt ovenfor dannes det et sjikt med tinn på overflaten av tenner som eksponeres for tinnfluorid. Hypersensitivt dentin vil kunne dekkes av et slikt tinnlag og hypersensitiviteten vil derved reduseres (13).
Vandige løsninger med tinnfluorid er mer effektive enn tannpasta. Det finnes også spesialpreparater med tinnfluorid løst i glyserol, der både effekten mot hypersensitivitet og stabiliteten av løsningene er meget gode.
Hva med tinnfluorid som kariesprofylaktikum?
I utgangspunktet (tidlig i 1950-årene) ble tinnfluoridtannpasta bare brukt i forebygging av karies. De andre egenskapene som er nevnt ovenfor, og som nå har stor interesse, fikk ingen oppmerksomhet. Grunnen var vel at karies var et overveldende problem, som hadde den aller høyeste prioritet. Det er kjent at den kariostatiske effekten skyldes tilstedeværelse av fluor, og ikke av tinn. Den kariesprofylaktiske effekt av tinnfluorid er dokumentert ved mer enn 40 kliniske eksperimenter og er således utvilsom (14). Et dyreforsøk utført på National Institute of Health i USA viser at tinnfluorid har noe bedre effekt enn NaF, men forskjellen var ikke signifikant (15). Et interessant poeng er at forskerne i sin tid antok at det var tinnfluoridets evne til å redusere tennenes løselighet i syre som var basis for dets kariostatiske effekt. Det ble gjennomført en omfattende jakt på mulige andre stoffer som kunne redusere tennenes løselighet. Men tinnfluorid ble funnet å være best (1). En del stoffer som riktignok nedsatte løseligheten av tenner, men som ikke inneholdt fluor, ble funnet ikke å ha kariostatisk effekt (1). En ren kariostatisk effekt kan nå oppnås billigere med MFP og NaF etter at abrasjonsmidler som ikke reagerer med fluorid ble tilgjengelige.
Mekanismen for tinnfluoridets evne til å redusere løseligheten av tenner er ikke kjent. Den skyldes imidlertid sannsynligvis kombinasjonen av fluor og lavt pH, uten at detaljene er kjent.
Hvilket indikasjonsområde har tannpasta med tinnfluorid i dag?
Den markerte antiplakkeffekten gjør at pasienter som har permanente problemer med munnhygienen kan være vel tjent med å anvende tinnfluoridtannpasta. Pasienter på sykehjem og sykehus, og geriatriske pasienter i sin alminnelighet, kommer i denne kategori. Ortodontipasienter med fast apparatur hører også hit, sammen med periodontittpasienter i vedlikeholdsfasen. Kanskje det kan sies at dette er en tannpasta for «godt voksne», der tilløp til periodontitt kan anes. Tinnfluorid er ikke så effektivt som klorheksidin, men later til å være mer effektivt enn triclosan. Tinnfluoridtannpasta vil også være til hjelp for pasienter som lider av dentinhypersensitivitet, som nevnt ovenfor.
Hva med effekt mot tannerosjoner?
Det er kjent at tinnfluorid reduserer løseligheten av emalje i syre. Da det ikke finnes noe annet tilgjengelig middel mot erosjoner, og da bruk av tinnfluoridtannpasta er uten bivirkninger (14), vil bruk av slik tannpasta være forsvarlig på erosjonspasienter. Bruk av tinnfluoridtannpasta på alvorlige tilfeller av tannerosjon sammen med individuelle skjeer, har vært prøvet av Bjarne Svatun, med subjektivt godt resultat (personlig kommunikasjon). Så dette er en metode som virker, med stor grad av sikkerhet. Applikasjonen kan i begynnelsen være daglig, men kan trappes ned etter hvert.
Den kliniske effekten av tinnfluoridtannpasta applisert på vanlig måte er ikke kjent. Dette beror på at metoder for klinisk utprøving foreløpig er hemmet av både tekniske og etiske problemer.
Hva med misfarging?
Det er kjent at tinnfluorid munnskyllemiddel kan gi en gulaktig misfarging. Dette skyldes at tinn oksideres fra stanno- til stannifluorid. Sistnevnte løsning kalles «mosaic gold» og brukes til rimelige «forgyllinger». Tannpasta med tilstrekkelig abrasivitet forårsaker ikke misfarging av betydning.
English summary
Rølla G.
Some properties of stannous fluoride - a new fluoride compound in Norway
390 – 2.
Stannous fluoride toothpaste has been used since the 1950s, mainly in the United States. Primarily a caries prophylactic agent, it was later introduced also as one agent against plaque and gingivitis. The tin part of the molecule has antibacterial properties. Stannous fluoride is thus unique, as it has both an anti caries effect and an antibacterial effect. Stannous fluoride reduces the solubility of enamel in acid and is now also used to prevent dental erosions. Stannous fluoride toothpaste has been used by millions of subjects for 20 years or more, and there is no reason to be concerned about diverse side effects.
Referanser
1. Muhler JC, Boyd TM, van Huysen G. Effect of fluorides and other compounds on the solubility of enamel. J Dent Res 1950; 29: 182 – 93.
2. Brudevold F, McCann HG, Nilsson R, Richardson B, Cocklea V. The chemistry of caries inhibition. Problems and challenges. J Dent Res 1967: 46; 37 – 45.
3. Tinanoff N. Progress regarding the use of stannous fluoride in clinical dentistry. J Clin Dent 1995; VI (spec issue): 37 – 40.
4. Tinanoff N. Review of the antibacterial action of stannous fluoride. J Clin Dent 1990; 2: 22 – 7.
5. Oppermann RV, Johansen JR. The effect of fluoride and non-fluoride salts of copper, silver and tin on the acidogenicity of dental plaque in vivo. Scand J Dent Res 1980; 88: 470 – 80.
6. Rölla G, Ellingsen JE. Clinical effects and possible mechanisms of action of stannous fluoride. Int Dent J 1994: 44: 99 – 105.
7. König KG. Dental caries and plaque accumulation in rats treated with stannous fluoride and penicillin. Helv Odontol Acta 1959; 3: 39 – 44.
8. Svatun B. Plaque inhibition effect of a dentifrice containing stannous fluoride. Acta Odontol Scand 1979; 36: 205 – 10.
9. Bay I, Rölla G. Morphologial studies of plaque formation and growth after NaF and Sn2 rinses. I: Rölla G, Sønju T, Embery G., red. Tooth surface interactions and preventive dentistry. London: IRL Press; 1981. pp 3 – 16.
10. Svanberg M, Rölla G. Streptococcus mutans in plaque and saliva after mouthrinsing with SnF2. Scand J Dent Res 1982; 90: 292 – 8.
11. Lilienthal B. The effect of stannous fluoride mouthwash on acid formation in the mouth and some observations on the mechanism of inhibition. Aust Dent J 1956; 1: 221 – 7.
12. Young A, Wåler SM, Jonski G, Rölla G. Effects of metal salts on the oral production of volatile sulfur-containing compounds. J Clin Periodontol 2001; 28: 233 – 8.
13. Thrash WJ, Dodds J, Jones DL. The effect of stannous fluoride on dentinal hypersensitivity. Int Dent J 1994; 44: 107 – 8.
14. White DJ. A «return» to stannous fluoride dentifrices. J Clin Dent 1955; VI (Spec issue): 9 – 36.
15. Rolla G, Amsbaugh SM, Monell-Torrens E, Ellingsen JE, Afseth J, Ciardi JE, Bowen WH. Effect of topical applications of stannous fluoride, stannous chloride and stannous tartrate on rat caries. Scand J Dent Res 1983; 91: 351 – 5.
Søkeord for nettversjon: www.tannlegetidende.no; Fluor; Karies; Kjemi; Munnpleiemiddel; Tannpasta.
Adresse: Bygdøy allé 56A, 0265 Oslo.