Nya behandlingsmetoder ur ett vetenskapligt och kliniskt perspektiv – en utvärdering
Författere
lektor, övertandläkare, odont. dr. Avd. för parodontologi, Odontologiska fakulteten, Sahlgrenska akademin vid Göteborgs universitet, Sverige
lektor, ph.d. Afdeling for Parodontologi, Odontologisk Institut, Det Sundhedsvidenskabelige Fakultet, Københavns Universitet, Danmark
Nya behandlingsmetoder introduceras kontinuerligt och tandläkaren måste kunna förlita sig på att den information som finns att tillgå är välgrundad och korrekt. Ofta är dock den vetenskapliga dokumentationen bristfällig och svårtolkad vilket gör det svårt att bedöma effekten av en ny behandling.
Utvärderingen av nya behandlingsmetoder bör bland annat omfatta jämförelser med redan etablerade metoder men en statistiskt signifikant skillnad mellan olika behandlingar innebär inte alltid att skillnaden är av klinisk betydelse.
Inom området parodontal infektionskontroll kan man förvänta sig att nya antiseptika och eventuellt även antiinflammatoriska substanser kommer att utvecklas i framtiden. Några substanser kommer sannolikt att ingå i tandkrämer. Lokal applicering av antimikrobiella substanser kommer troligen att utvecklas så att tilläggseffekten blir av mer avgörande klinisk betydelse jämfört med i dag. Trots de nya behandlingsmetoderna som kommer att erbjudas kommer patientens vilja och förmåga att upprätthålla en god munhygien fortfarande att vara av helt avgörande betydelse för det långsiktiga behandlingsresultatet.
Behandling av gingivit och parodontit inriktar sig i första hand mot att reducera ett infektionstillstånd runt tänderna till en nivå där fortsatt nedbrytning av de parodontala vävnaderna kan hejdas. Infektionskontrollen bygger på olika behandlingsmetoder som syftar till att eliminera/reducera förekomsten av bakteriebeläggningar på tänderna, plack.
Etablerade behandlingsmetoder baseras på att avlägsna bakteriebeläggningarna med mekaniska medel, det vill säga genom depuration med handinstrument eller ultraljudsinstrument. Metoden är emellertid tekniskt krävande och tidsödande och resultaten är därför ofta mycket varierande. Parodontalkirurgi kan i situationer där åtkomligheten för depuration av rotytan är försvårad förbättra behandlingsresultatet (1, 2).
För att långsiktigt uppnå ett lyckat behandlingsresultat krävs dessutom att patienten upprätthåller en god munhygien. Efter en parodontitbehandling är det därför av yttersta vikt att patienten involveras i ett individuellt anpassat program för återbesök för att tidigt kunna upptäcka och åtgärda tecken på begynnande recidiv (3).
På grund av svårigheterna att avlägsna plack och tandsten kan det ibland vara indicerat att kombinera den mekaniska behandlingen med antiseptika eller antibiotika. För supragingival infektionskontroll finns ett antal antiseptiska substanser som ingår i både tandkräm och munsköljningsmedel med dokumenterad effekt på plack (4 – 6).
Under senare år har även nya beredningsformer för antibiotikabehandling utvecklats som är speciellt anpassade för lokal behandling av parodontit (7, 8). Genom lokal applicering direkt i tandköttsfickan når man avsevärt högre koncentrationer av antibiotika i det subgingivala bakterieplacket jämfört med systemisk behandling. Samtidigt är den systemiska påverkan på patienten minimal.
Från att tidigare enbart ha inriktat behandlingen på att försöka eliminera den parodontala infektionen har intresset fokuserats på att utveckla behandlingsmetoder som minskar de negativa effekterna av behandlingen, till exempel gingivala retraktioner, isande tandhalsar et cetera. Dessa behandlingsmetoder möjliggör även återbildandet av förlorad parodontal stödjevävnad. Patienterna ställer också större krav på att den parodontala behandlingen inte enbart ska bota sjukdomen utan vill även att resultatet blir estetiskt acceptabelt.
GTR (guided tissue regeneration), populärt kallat membranbehandling, är ett exempel på en teknik som syftar till att försöka återskapa förlorat parodontalt fäste (9, 10). Behandlingskonceptet bygger på principen att skapa förutsättningar för rotcement och rothinna att växa in i sårområdet efter parodontalkirurgi, etablera förbindelse med den depurerade rotytan och därigenom skapa ett nytt fäste.
Ytterligare en regenerativ behandlingsmetod som utvecklats under senare år bygger på principen att man i samband med parodontalkirurgi applicerar ett emaljprotein på den depurerade rotytan (11). Proteinerna som frisätts i samband med rotutvecklingen påverkar den omgivande vävnaden att börja bilda rotcement och rothinna.
Utvärdering av nya behandlingsmetoder
Hur utvärderar man en ny produkt eller en ny behandlingsstrategi? Vilka mått på parodontal sjukdom och/eller sjukdomsprogression bör man använda och hur skiljer sig patientens subjektiva värdering från tandläkarens «objektiva» värdering av behandlingsresultatet? Tandförlust är den yttersta konsekvensen av parodontit. Personer med obehandlad parodontit förlorar i genomsnitt 0,2 – 0,4 tänder per år, jämfört med 0,01 – 0,05 tänder per år hos behandlade individer (12, 13). Variationen är emellertid stor och ett fåtal individer svarar ofta för merparten av tandförlusterna (14, 15).
Om tandförlust ska användas som mått på parodontitsjukdom vid utvärdering av en behandlingsmetod krävs det mycket långa studier. Tandförlust måste därför ersättas med undersökningsparametrar som långt tidigare speglar förekomsten av parodontal sjukdom och sjukdomsprogression samt i förlängningen risk för tandförlust. Exempel på sådana parametrar (så kallade surrogatparametrar) är fästenivå, fickdjup, blödning vid sondering, pus, mobilitet, gingivala retraktioner och förändring av bennivån på röntgen. Samtliga registreringsmetoder speglar på olika sätt och i varierande grad förekomst av parodontal sjukdom. Det är dock egentligen bara fästenivåmätning och förändring av bennivån på röntgen som är ett direkt mått på destruktion av tandens fäste. Övriga parametrar beskriver förhållanden hos de parodontala vävnaderna som kan hänföras till olika grad av inflammation men de avspeglar inte sjukdomsprogression i dess strikta bemärkelse, det vill säga fästeförlust.
Tandförlust som mått på parodontal sjukdomsprogression är en så kallad true endpoint. En förändring i exempelvis blödning, fickdjup eller fästenivå är i sin tur exempel på kliniska parametrar där man använder sig av surrogate endpoints för att beskriva sjukdomsprogression. Det är emellertid ett problem att vi bara har en begränsad kunskap om hur god korrelationen är mellan en true endpoint-parameter och den surrogatparameter som vi använder oss av. Det kan medföra att ekonomiska resurser inom vården används på ett onyanserat sätt. Ett exempel är att man, genom att fördela resurserna jämnt över hela behandlingspanoramat, riskerar att få för lite resurser till viktigare behandlingsinsatser. Med andra ord; det finns risk för överbehandling eftersom effekten av den behandlingen som satts in har en liten betydelse för true endpoint-variabeln.
I Tabell 1 ges exempel på hur stor risken är att förlora parodontalt fäste vid närvaro respektive frånvaro av till exempel pus, blödning eller ett fickdjup ³ 6 millimeter. Begreppet sensitivitet anger sannolikheten för fortsatt fästeförlust vid ett positivt fynd av en specifik parameter. Således är risken för att förlora fäste 30 procent för en yta som blöder vid sondering (16). Specificitet anger å andra sidan hur stor sannolikheten är att inte förlora fäste om man inte finner pus, blödning eller fickdjup ³ 6 millimeter. Uppenbarligen är tecken på sjukdom inte det samma som sjukdomsprogression medan frånvaro av sjukdomstecken i det närmaste garanterar bibehållet parodontium.
|
Sensitivitet |
Specificitet |
|---|---|---|
Pus |
3 |
92 |
Blödning vid sondering |
30 |
99 |
Fickdjup ³ 6 mm |
25 |
92 |
Krav på vetenskaplig dokumentation
Att värdera nya forskningsresultat kan ibland vara svårt speciellt om man inte har stor erfarenhet av att tolka vetenskapliga publikationer eller rapporter. Ofta får vi vår huvudsakliga information via tillverkaren i form av mer eller mindre sakligt underbyggda prospekt, som utlovar goda behandlingsresultat. För att kunna bedöma effekten av ett nytt behandlingskoncept måste den vetenskapliga dokumentationen vara baserad på studier som uppfyller vissa krav beträffande utformning, genomförande och analys. Många studier uppfyller emellertid inte dessa krav. Det innebär att det ibland inte går att dra några säkra slutsatser om värdet av en ny behandling (17).
En vetenskapligt korrekt utformad klinisk studie bör uppfylla kriterierna för en så kallad RCT-studie (randomized controlled trial). Samtliga individer som uppfyller vissa specifika krav avseende ett antal förutbestämda egenskaper, så kallade inklusionskriterier (se faktaruta I) ska ha samma chans att ingå i testgruppen eller en motsvarande kontrollgrupp (randomized). Kontrollgruppen, som oftast får genomgå en redan etablerad behandling, är väsentlig för att rätt kunna utvärdera effekten av den nya behandlingsmetoden (controlled) (17).
Faktaruta I
Inklusionskriterier:
till exempel ålder, kön, allmän hälsa, antal tänder, förekomst av parodontit)
I vissa fall gör man avkall på de vetenskapliga kraven på slumpmässigt urval enligt principerna för en RCT-studie genom att till exempel rekrytera nya försökspersoner till en studie allt eftersom de söker kliniken för behandling. Den aktuella patientgruppen utgör således inte ett slumpmässigt urval av patienter i allmänhet utan är selekterad. Detta gäller kanske särskilt om försökspersonerna samtidigt erbjuds en ekonomiskt överkomlig behandling eller, alternativt, att de bor i närheten av den forskningsinstitution där den vetenskapliga undersökningen ska genomföras. Resultatet av en sådan studie, så kallad case series, kan därmed inte sägas gälla för patienter i allmänhet utan enbart för den typ av patienter som deltagit i undersökningen. Man kan därför inte applicera behandlingsresultat som baseras på en specifik patientgrupp och förvänta sig motsvarande effekter hos en grupp individer med andra förutsättningar vad gäller till exempel ålder, könsfördelning, utbildning, grad av sjukdom och så vidare.
För närvarande pågår i Sverige ett omfattande arbete med att utvärdera olika behandlingsmetoder inom odontologin. SBU, Statens beredning för medicinsk utvärdering, har bland annat till uppgift att, baserat på den befintliga vetenskapliga litteraturen, utvärdera effekten av ett antal specifika behandlingsmetoder. För att kunna hävda att en behandlingsmetod har en viss påstådd effekt krävs enligt SBU att den är evidensbaserad (evidence based) det vill säga undersökningarna måste uppfylla vissa krav för att godkännas som vetenskapligt underlag för påståendet (18).
När ett flertal undersökningar uppfyller kraven på god vetenskaplig utformning men när resultaten av dessa undersökningar var för sig inte kan utgöra grund för en tillförlitlig utvärdering, till exempel på grund av för litet antal försökspersoner, kan man använda sig av metaanalys. Metaanalys innebär att resultaten från flera undersökningar med liknande utformning och frågeställning vägs samman och analyseras med hjälp av specifika statistiska metoder. Denna form av analys kan vara värdefull när det finns en relativt omfattande vetenskaplig dokumentation inom ett specifikt område. Med hjälp av metaanalys kan man dra mer tillförlitliga slutsatser om utfallet av en viss behandlingsmetod. Den samlade konklusionen baserar sig då på undersökningar som genomförts vid olika oberoende forskningsinstitutioner. Vid så kallade multicenterstudier följer flera forskningscentra samma undersökningsprotokoll. Fördelen med denna metod är dels att det patientunderlag som utgör stickprovet är mer representativt samt att man även kan se hur stor samstämmigheten blir mellan olika centra (17).
Vid multicenterstudier kan man dessutom lättare få ett tillräckligt stort antal patienter med till exempel en speciell åkomma och därmed kunna göra pålitligare statistiska analyser.
Klinisk och statistisk signifikans
I de flesta vetenskapliga studier redovisas undersökningsresultaten med hjälp av olika statistiska analysmetoder. Om analysen visar att skillnaden mellan olika behandlingsmetoder är statistiskt signifikant tas detta oftast som intäkt för att den ena behandlingsmetoden är överlägsen den andra. Problemet är emellertid att den statistiska analysen bygger på statistiskt matematiska samband och antaganden som inte alltid speglar vad som anses vara väsentligt ur klinisk synpunkt. Ett statistiskt signifikanstest används då man vill undersöka om man kan påstå att det finns en skillnad mellan två eller flera behandlingar eller om den observerade skillnaden lika väl kan bero på slumpen. Det är i detta sammanhang viktigt att vara medveten om att ju fler individer som deltagit i studien desto mindre kliniska skillnader kan påvisas som statistiskt signifikanta. Resultatet av en statistisk signifikansanalys är alltså i stora delar avgörande av hur många individer som ingått i undersökningen.
Det är väsentligt att tolkningen av resultaten baseras på den statistiska analysen men avgörande är vilken klinisk betydelse den nya behandlingsmetoden har. En skillnad i fickdjup på några tiondels millimeter mellan olika behandlingsmetoder kan vara statistiskt signifikant men kan kanske sakna betydelse i ett kliniskt perspektiv.
Vid planering av en klinisk studie är det därför väsentligt att man bestämmer vilken skillnad i behandlingsresultat man anser vara av kliniskt intresse. Med hjälp av en statistisk metod, en så kallad power-analys, kan man beräkna hur många individer som ska ingå i studien för att man med en på förhand bestämd säkerhet ska kunna upptäcka skillnaden. Power-analysen är följaktligen ett viktigt instrument vid beräkning av stickprovsstorleken (17).
Gruppmedelvärde eller enstaka tandköttsficka
Vid redovisning av forskningsresultat presenteras dessa ofta i form av medelvärde och det framgår inte alltid hur enskilda individer eller enstaka tandköttsfickor reagerat på en behandling. Vissa individer/tandköttsfickor svarar mycket dåligt alternativt mycket bra på behandlingen. För att undvika att «avvikande» behandlingsresultat döljs bakom medelvärden bör resultaten även redovisas i form av tabeller och diagram där effekten av behandlingen hos den enskilde individen alternativt tandköttsfickan framgår. Exempelvis kan effekten av behandlingen beskrivas som en förskjutning av grupperingen/fördelningen av individer i olika parodontala sjukdomskategorier. Som ett annat exempel kan effekten av två olika behandlingsregimer illustreras med hjälp av ett diagram som beskriver fästenivåförändringen i relation till det initiala fickdjupet, till exempel 3 mm, 4 – 6 mm och ³ 7 mm (Fig. 1) (19). Denna form av beskrivande statistik ger en mer nyanserad bild av effekten av de olika behandlingarna jämfört med att, som oftast, presentera förändringen av fästenivån uttryckt som ett medelvärde för respektive behandling.
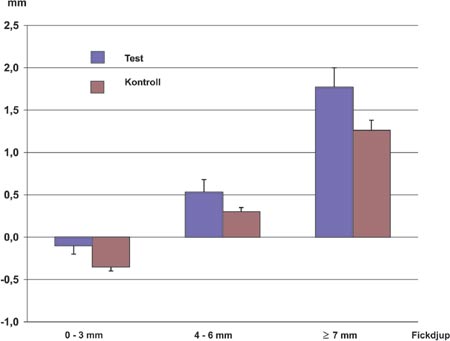
Fig 1. Fästenivåförändring för olika fickdjupskategorier efter 12 månader.
Ett annat sätt att beskriva undersökningsresultatet är med hjälp av ett konfidensintervall (CI). Konfidensintervallet anger de gränser som med en förutbestämd säkerhet kan förväntas innefatta det sanna värdet, till exempel den genomsnittliga fickdjupsreduktionen eller fästevinsten för en given parodontalbehandling. Oftast anger man ett 95-procentigt konfidensintervall, det vill säga det är bara 5 procents risk för att det sanna (riktiga) värdet inte omsluts av intervallets övre och nedre gränser. Om man vill jämföra två behandlingsmetoder och finner att den genomsnittliga skillnaden i fickdjup är 0,3 millimeter och att det motsvarande 95-procentiga konfidensintervallet för skillnaden mellan behandlingarna beräknas ha en nedre gräns på 0,1 millimeter och en övre gräns på 0,7 millimeter ser vi att konfidensintervallet omsluter 0 (noll). Vi kan därför säga att det i verkligheten inte finns någon skillnad på effekten av de två behandlingarna. Hade gränserna inte omslutit 0 kan man i gengäld säga att det kan antas (med 95 % säkerhet och 5 % osäkerhet) att det föreligger en skillnad mellan behandlingarna. Lägg märke till att man kan uttala sig om storleksordningen av den genomsnittliga skillnaden men inte vad den är i verkligheten. Det sista exemplet illustrerar med all önskvärd tydlighet att en skillnad mycket väl kan vara statistiskt hållbar men att den uppnådda effekten trots det inte förtjänar mycket uppmärksamhet ur klinisk synpunkt.
Det är också viktigt att man väljer rätt population när man vill studera effekten av en viss behandling. För att undersöka effekten av en ny behandlingsmetod för förbättrad munhygien bör man lämpligen välja personer ur en grupp av individer som har en bristfällig munhygien. Hos individer med god munhygien kan man knappast förvänta sig att finna några skillnader mellan olika behandlingar. Vid undersökningar med sådana försökspersoner kan det vara svårt att visa att exempelvis en tandkräm som innehåller ett antiseptiskt medel har någon effekt. En konsekvens av detta är att undersökningar med munhygieniska produkter förläggs till mindre utvecklade delar av världen där förekomsten av plack och gingivit är mer förekommande och behandlingseffekten blir mer uttalad. Motsvarande effekter kan däremot inte påvisas hos individer i mer utvecklade delar av världen där nivån på den egna munhygienen och därmed munhälsan är betydligt högre.
Nya behandlingsmetoder och etik
Det måste vara av avgörande betydelse att de nya behandlingsmetoder vi applicerar på våra patienter är lika bra (eller bättre) som etablerade behandlingsmetoder. Det bör vara självklart för varje vårdgivare att inte introducera nya behandlingar innan det klart framgår att patienten inte kommer att lida någon skada och att den nya behandlingsmetoden medför att patientens tillstånd förbättras eller åtminstone inte försämras jämfört med etablerade metoder. En annan aspekt på införandet av nya behandlingsmetoder är att även om de inte medför ett bättre behandlingsresultat kanske de är mindre kostsamma alternativt mindre smärtsamma eller mer tidsbesparande för patienterna. Nya behandlingsmetoder tenderar dock, oavsett hur dokumenterad den påstådda effekten är, att vara relativt dyra.
Genom att applicera ett vetenskapligt betraktelsesätt vid prövning av nya behandlingsmetoder kan man göra en bättre bedömning av tillförlitligheten av dessa metoder. Därmed kan man förhindra att metoder som efter en tids användning visar sig vara overksamma eller mer eller mindre skadliga etableras. Inom det odontologiska området hittar vi exempel på experimentella studier som med nutidens glasögon får betraktas som oetiska, även om exempel på behandlingar som varit direkt skadliga knappast funnits i modern tid.
Den snabba teknologiska utvecklingen har även medfört att det har introducerats behandlingsmetoder där dokumentationen av den påstådda effekten är mer eller mindre felaktig. Det finns exempel på laserutrustning för parodontalbehandling där CE-märkningen uppfattats som ett officiellt godkännande för användning. Egentligen betyder denna märkning endast att apparaturen uppfyller bestämda normer för de elektriska komponenterna för att tandläkare och patient ska slippa riskera livet i samband med behandling. (Samma normer gäller för övrigt för dammsugare och tvättmaskiner.)
Utvärdering av olika metoder för infektionskontroll
Manuell borste jämfört med elektrisk tandborste
Mekanisk supragingival plackkontroll är den viktigaste enstaka åtgärden vid behandling av gingivit och parodontit. Plackkontrollen har en avgörande betydelse för en effektiv rengöring av tänderna. Mot bakgrund av den kunskapen kombinerat med tekniska svårigheter och patienternas långsiktiga medverkan (20) har ett antal olika modeller av elektriska tandborstar utvecklats.
För att kunna värdera den plackavlägsnande effekten av en elektrisk tandborste är det väsentligt att undersökningen utformas på ett sådant sätt att det finns en rimlig chans att besvara frågeställningen. Försökspersonerna bör vara individer som inte har en optimal munhygien. Enligt kraven på en RCT-studie ska man alltså jämföra effekten av eltandborste (test) med effekten av en etablerad metod, i detta fall manuell tandborstning (kontroll).
Ett flertal studier av varierande utformning har genomförts under senare år. Överlag visar resultaten att de elektriska tandborstarnas plackavlägsnande effekt är bättre jämfört med mekanisk tandborstning (21, 22).
Hur stor skillnad talar man då om och vilka undersökningsparametrar har man använt sig av? Även om en elektrisk tandborste visar sig kunna avlägsna plack bättre än en manuell tandborste är det viktigare att undersöka hur stor behandlingseffekten är på gingivit och i förlängningen även på parodontit. I ett exempel från en undersökning där man jämfört effekten av elektrisk och manuell tandborste (23) drog man slutsatsen att den elektriska tandborsten signifikant reducerade plack och gingivit efter tre månader jämfört med en manuell tandborste. Skillnaden i plack- och gingivitreduktion efter tre månader var 7 respektive 4 procent mellan de båda borstmetoderna (Tabell 2). Skillnaden i plack och gingivit speciellt på approximalytor var densamma (8 respektive 4 %). Gingivit uttryckt som gingivalindex (GI) reducerades approximalt med 0,17 enheter i gruppen som använde elektrisk tandborste jämfört med 0,14 enheter hos motsvarande ytor i kontrollgruppen (Fig. 2). Skillnaden i gingivitreduktion mellan de båda borstmetoderna var statistiskt signifikant och kan även uttryckas som att försökspersonerna i eltandborstgruppen efter 3 månader uppvisade 3 – 4 fler approximalytor med mindre inflammation jämfört med kontrollgruppen. Det är med andra ord väsentligt att man gör en tolkning av den kliniska relevansen av det statistiska undersökningsresultatet. Generellt kan man säga att man alltid skal vara uppmärksam vid tolkningen av procenttal. Åttio procent av ingenting är ingenting. Man bör alltså se till den faktiska förändringen av en klinisk parameter och vilken klinisk betydelse den uppmätta förändringen har. En reduktion i blödningsindex (se faktaruta II) från 4 till 3 procent är en reduktion med 25 procent men kan knappast anses kliniskt betydelsefull.
Faktaruta II
Blödningsindex:
Blödningsindex uttrycks i allmänhet i procent, det vill säga; det procentuella antal ytor som blöder vid till exempel ficksondering.
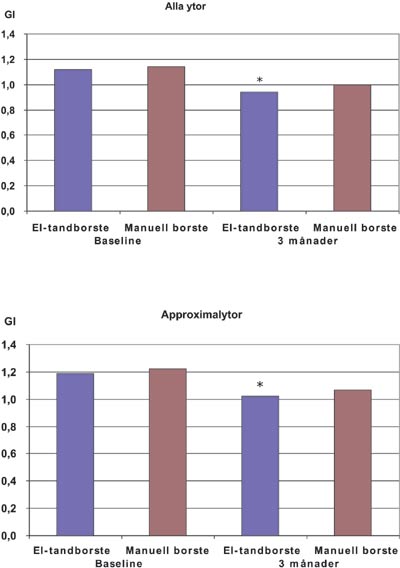
Fig. 2. Förändring av gingivalindex (GI) Baseline – 3 månader. * = signifikant skillnad mellan el-tandborste och manuell tandborste (p < 0,05).
Alla ytor |
Approximalytor |
|||
|---|---|---|---|---|
El-tandborste |
Manuell borste |
El-tandborste |
Manuell borste |
|
Plack |
15* |
8 |
15* |
7 |
Gingivit |
16* |
12 |
14* |
12 |
Blödning |
65 |
56 |
64 |
55 |
Antibiotikabehandling
Behandling av infektionssjukdomar innefattar ofta antibiotikaterapi. Mot bakgrund av parodontitens otvetydiga koppling till bakteriebeläggningar på tänderna och i tandköttsfickan är det naturligt att även vid detta tillstånd överväga att använda antibiotika.
Generell eller systemisk antibiotikabehandling i kombination med konventionell mekanisk behandling har använts under många år. Det råder en enad uppfattning om att generell antibiotikabehandling som komplement till konventionell behandling av kronisk parodontit inte märkbart förbättrar behandlingsresultatet. I ett flertal studier har man funnit att tilläggseffekten av antibiotika på till exempel den kliniska fästenivån i genomsnitt är cirka 0,3 – 0,4 millimeter jämfört med konventionell behandling (19, 24 – 26).
Lokal behandling med antibiotika och antiseptika
Ett antal nya behandlingsmetoder har utvecklats för lokal applicering av antiseptika och antibiotika i tandköttsfickan. Ett av problemen som förknippas med denna form av behandling är att det bildas ett gingivalt exsudat i samband med den parodontala infektionen. Mängden exsudat som produceras i en inflammerad tandköttsficka per timme kan motsvara upp till 40 gånger tandköttsfickans totala volym. Det medför i sin tur att när man applicerar en terapeutisk substans subgingivalt utsätts medlet omedelbart för en utspädningseffekt och koncentrationen sjunker snabbt under terapeutiska nivåer (27). Vissa antiseptiska ämnen som till exempel klorhexidin neutraliseras dessutom av de proteiner som finns i gingivalt exsudat.
Genom att låta de terapeutiska ämnena ingå i speciella bärarsubstanser som gör att det aktiva ämnet utsöndras långsamt kan man upprätthålla mycket höga koncentrationer av den terapeutiska substansen i tandköttsfickan under en längre tidsperiod.
De antibiotika för lokal administrering i tandköttsfickan som i dag finns på marknaden är Elyzol® dental gel (som innehåller 25 % metronidazol) och Atridox® (som innehåller 8,8 % doxycyklin, ett tetracyklin-derivat). Ytterligare lokala antibiotika är under utprovning och man kan förvänta sig en fortsatt utveckling i framtiden.
Inom gruppen antiseptika för lokal subgingival applicering finns PerioChip®, ett resorberbart inlägg som innehåller klorhexidin. PerioChip appliceras i tandköttsfickan och frisätter klorhexidin under 7 – 10 dagar.
Kännetecknande för samtliga preparat är att de innehåller en liten mängd aktiv substans. PerioChip innehåller exempelvis 2,5 mg klorhexidin per chip vilket ska jämföras med den mängd klorhexidin man tillför dagligen vid munsköljning (30 – 40 mg).
Även för Atridox är den totala dosen låg (cirka 40 mg) under de cirka 10 dagar som medlet utsöndras. Det ska jämföras med cirka 1 000 mg vid systemisk administrering. Trots de relativt små mängderna aktiv substans som finns i chipset respektive gelen medför tekniken att man når betydligt högre koncentrationer i tandköttsfickan jämfört med till exempel subgingival spolning med klorhexidin eller systemisk administration av doxycyklin.
Elyzol dental gel – I studier där man undersökt tilläggseffekten av elyzolbehandling i kombination med subgingival depuration redovisas en viss tilläggseffekt jämfört med enbart depuration. Griffiths et al. (28) visade att tilläggseffekten till depuration uttryckt som fickdjupsreduktion var 0,5 millimeter, och 0,4 millimeter uttryckt som klinisk fästevinst samma storleksordning som tilläggseffekten vid systemisk administrering av metronidazol. Av fickorna i depurationsgruppen blödde 42 procent vid sondering, att jämföras med 35 procent hos de patienter som även behandlats med Elyzol-gel. Skillnaden i reduktion av blödning mellan behandlingarna var 9 procent efter 9 månader. Även det resultatet bör vägas in vid en värdering av den kliniska betydelsen av lokal antibiotikabehandling (28).
För att kunna bedöma tillförlitligheten av resultaten är det viktigt att försöket är väl utformat och genomfört. Kliniska parametrar som till exempel fickdjupsmätning och fästenivåmätning är behäftade med mätfel. I den refererade undersökningen (28) försökte man genomföra alla kliniska registreringar så identiskt som möjligt. Med hjälp av individuellt framställda bitskenor där varje mätpunkt definierades med en markering i skenan kunde varje registrering göras vid samma mätpunkt vid varje undersökningstillfälle. Studien var även upplagd enligt en så kallad split mouth-design. Det innebar att ena halvan av käken behandlades med depuration och Elyzol dental gel och andra halvan med enbart depuration. Varje patient var alltså sin egen kontroll. En fördel eftersom de individuella skillnaderna mellan hur olika individer reagerar på en behandling kan vara stora.
Doxycyklin-behandling – Docxycyklin är ett tetracyklinderivat, som ingår som aktiv beståndsdel i Atridox. Atridox appliceras lokalt i fickan efter genomförd depurationsbehandling. Till skillnad mot Elyzol dental gel upprätthåller Atridox® höga koncentrationer av doxycyklin i tandköttsfickan under cirka 10 dagar. Doxycyklin når så höga koncentrationer lokalt i tandköttsfickan att substansen, som normalt är bakteriostatisk vid systemisk administrering, får baktericida egenskaper.
I en nyligen publicerad studie (29), där man ville undersöka effekten av Atridox som tillägg till konventionell depuration på fickor ³ 5 millimeter rapporterades att Atridox-behandling inte gav signifikant större fickdjupsreduktion men signifikant större fästenivåvinst jämfört med enbart depurationsbehandling. Skillnaden i fickdjupsreduktion och fästenivåvinst 3 månader efter avslutad behandling var i medeltal 0,2 respektive 0,3 millimeter för de 5 millimeter djupa fickor som behandlats med Atridox jämfört med motsvarande fickor som enbart genomgått depurationsbehandling. Uttryckt i procent uppvisade 38 procent av alla behandlade fickor i Atridox-gruppen en fästenivåvinst på ³ 2 millimeter jämfört med 30 procent i depurationsgruppen.
Antalet fickor ³ 5 millimeter som kvarstod efter respektive behandling efter 3 månader var 42 procent i Atridox-gruppen och 50 procent i depurationsgruppen. Skillnaden i behandlingseffekt efter 3 månader var således liten och i nivå med den tilläggseffekt man får vid systemisk antibiotikabehandling.
Lokal behandling med klorhexidin, PerioChip är en relativt ny behandlingsmetod (30, 31). I en undersökning genomförd av Soskolne et al. (30) framkom att behandling av tandköttsfickor ³ 5 millimeter genom depuration i kombination med PerioChip reducerade fickdjupet mer jämfört med enbart depurationsbehandling. Fickdjupsreduktionen var i genomsnitt 0,4 millimeter större för fickor som behandlades med PerioChip och depuration jämfört med fickor som enbart behandlades med depuration. Författarna kunde även visa att tilläggseffekten var större i djupare fickor, ³ 7 mm, det vill säga fickor som normalt är svåra att depurera. Den sistnämnda informationen är intressantare ur klinisk aspekt då djupa fickor är mer benägna att recividera.
För att ytterligare kunna utvärdera effekten av behandling med PerioChip är det emellertid lämpligt att jämföra effekten med andra närliggande behandlingsmetoder som lokal antibiotikabehandling. Salvi et al. (32) jämförde effekten av PerioChip med lokalbehandling med Elyzol och Atridox. Samtiga patienter i studien genomgick först konventionell depurationsbehandling. Efter 2 – 4 månader undersöktes alla patienterna på nytt och samtliga fickor ³ 5 millimeter behandlades därefter antingen med PerioChip, Elyzol eller Atridox. Vid utvärderingen efter 3 månader fann man statistiska skillnader mellan respektive behandlingar men skillnaderna var små ur klinisk aspekt (Tabell 3). Det som dock gör undersökningen svår att tolka är att ingen av fickorna ³ 5 millimeter som kvarstod efter den initiala depurationsbehandlingen behandlades igen med enbart depuration. Det innebär att man inte kunde utvärdera effekten av de olika tillläggsbehandlingarna med konventionell depurationsbehandling. Sammantaget kan man konstatera att tilläggseffekten av lokal behandling med antibiotika/antiseptika är liten ur klinisk synpunkt och att den inte nämnvärt skiljer sig från de effekter man får vid till exempel systemisk behandling med antibiotika (33).
Behandling |
Baseline |
4 månader |
Förändring |
Förändring vs Atridox |
|---|---|---|---|---|
Elyzol |
5,01 0,35 |
4,98 0,34 |
0,03 0,10 |
p = 0,014 |
PerioChip |
5,25 0,46 |
5,09 0,42 |
0,16 0,12 |
p = 0,078 |
Atridox |
4,61 0,26 |
4,28 0,23 |
0,33 0,23* |
|
Parodontal regeneration – Behandling med GTR (membranbehandling) och/eller emaljprotein (Emdogain®) görs i situationer där konventionell parodontalkirurgisk behandling inte förväntas ge ett acceptabelt behandlingsresultat på grund av skadans omfattning eller av estetiska skäl. Metaanalys av ett flertal undersökningar har visat att behandling av angulära bendefekter med regenerativa tekniker i genomsnitt ger 1 millimeter mer kliniskt fäste jämfört med motsvarande behandling utan regenerativ teknik. Motsvarande tillläggseffekt har rapporterats vid behandling av buccala furkaturer grad II på 1:a molarer i underkäken. Regenerativ behandling av approximala furkaturer på överkäksmolarer har dock inte uppvisat bättre läkning jämfört med konventionell behandling (11, 34 – 36).
Även om dagens regenerativa metoder tycks ge ett bättre behandlingsresultat jämfört med konventionell behandling är metoderna teknikkänsliga. Trots mycket kontrollerade undersökningar kan man inte förvänta sig en större tilläggseffekt än cirka 1 millimeter fästevinst. Skadans omfattning är även av betydelse för läkningen. En grund och vid benficka med få kvarvarande benväggar har sämre förutsättningar för att läka oavsett om man använder sig av regenerativ teknik eller inte. Smala, djupa defekter med flera kvarvarande benväggar har emellertid potentialen att läka väl även vid konventionell behandling förutsatt att rotytan är åtkomlig för depuration. I sådana fall är kanske ytterligare 1 millimeters fästevinst av mindre klinisk betydelse och regenerativ behandling bör då inte övervägas. Utvärdering av kliniska studier på människa baseras enbart på kliniska registreringar av fästevinst vilket inte kan tas som intäkt för att man fått tillbaka ett intakt bindvävsfäste. Det kan mycket väl vara fråga om konventionell läkning med ett långt kontaktepitel mellan roten parat med en mer eller mindre benutfylld intraosseös defekt.
Det finns inte heller något vetenskapligt belägg för att en parodontal skada som läkt efter regenerativ behandling skulle vara mer motståndskraftig mot parodontitrecidiv jämfört med läkning efter konventionell behandling.
Nya behandlingsmetoder i framtiden
Inom området parodontal infektionskontroll kan man förvänta sig att nya antiseptika och eventuellt även antiinflammatoriska substanser utvecklas. Några substanser kommer sannolikt att ingå i tandkrämer. Lokal applicering av antimikrobiella substanser kommer troligen att utvecklas så att tilläggseffekten blir av mer avgörande klinisk betydelse jämfört med i dag.
Den andra stora utmaningen i framtidens behandlingspanorama är att utveckla nya regenerativa behandlingsmetoder för att återbilda både mjukvävnad och ben med tillhörande parodontalt fäste. Möjligheterna att återskapa ben och parodontalt fäste är i dag begränsade och beroende av utseendet på den skada som uppkommit. Kvarstående benväggar är till exempel avgörande för hur mycket ben som ska kunna återbildas. En tand som förlorat parodontalt fäste till samma nivå vid samtliga tandytor (så kallad horisontell nedbrytning) kan med dagens behandlingsmetoder inte återfå det ursprungliga fästet oavsett vilken behandling som sätts in.
Trots de nya behandlingsmetoder som framtiden kommer att erbjuda kommer dock patientens vilja och förmåga att upprätthålla en god munhygien fortfarande att vara av helt avgörande betydelse för det långsiktiga behandlingsresultatet.
English summary
Ramberg P, Stoltze K.
Evaluation of new treatment methods from a scientific and clinical point of view
92 – 8.
Treatment of gingivitis and periodontitis focuses on reduction of inflammation to a level where further breakdown of the periodontal tissues is arrested. Most established methods of treatment are, however, technically demanding and time-consuming. Several new treatment methods include various adjunctive measures, i.e. electric toothbrushes as well as antiseptics and antibiotics for subgingival application to improve the effect of the mechanical treatment.
New treatment methods should be developed and documented in accordance with a high level of scientific standards. When a clinical trial is designed, it is important that the outcome of the application of a new treatment method can be weighed against an established method. Moreover, the periodontal condition of the subjects recruited for the trial and the periodontal parameters selected for examination must match the treatment method under investigation.
The fact that a statistical analysis shows a significant difference when the outcomes of various treatments are compared does not necessarily mean that the difference is of clinical importance. Whether statistical analysis results in a significant difference or not may depend on several factors, i.e. the number of patients included in the study as well as their initial periodontal condition.
Referenser
1. Caffesse RG, Sweeney PL, Smith BA. Scaling and root planing with and without periodontal flap surgery. J Clin Periodontol 1986; 13: 205 – 10.
2 Lindhe J, Westfelt E, Nyman S, Socransky SS, Heijl L, Bratthall G. Healing following surgical/non-surgical treatment of periodontal disease: A clinical study. J Clin Periodontol 1982; 9: 115 – 28.
3. Axelsson P, Lindhe J. The significance of maintenance care in the treatment of periodontal disease. J Clin Periodontol 1981; 8: 281 – 94.
4. Kornman KS. Antimicrobial agents. State-of-the-sience review. In: Löe H, Kleinman DV, editors. Dental plaque control measures and oral hygiene practices. Oxford-Washington D.C.: IRL Press Ltd.; 1986. p. 121 – 42.
5. Van der Ouderaa FJG. Anti-plaque agents. Rationale and prospects for prevention of gingivitis and periodontal disease. J Clin Periodontol 1991; 18: 447 – 54.
6. Ramberg P, Furuichi Y, Sherl D, Volpe AR, Nabi N, Gaffar A, et al. The effect of triclosan on developing gingivitis. J Clin Periodontol 1995; 22: 442 – 8.
7. Greenstein G, Polson A. The role of local drug delivery in the management of periodontal disease: a comprehensive review. J Periodontol 1998; 69: 507 – 20.
8. Kinane DF, Radvar M. A six-month comparison of three periodontal local antimicrobial therapies in persistent periodontal pockets. J Periodontol 1999; 70: 1 – 7.
9. Gottlow J. Periodontal regeneration. In: Lang NP, Karring T, editors. Proceedings of the 1st European Workshop on Periodontology. London: Quintessence; 1994. p. 172 – 92.
10. Hammarström L. Enamel matrix, cementum development and regeneration. J Clin Periodontol 1997; 24: 658 – 68.
11. Heijl L, Heden G, Svärdström G, Östgren A. Enamel matrix derivative (Emdogain®) in the treatment of intrabony periodontal defects. J Clin Periodontol 1997; 24: 705 – 14.
12. Wennström JL, Serino G, Lindhe J, Eneroth L, Tollskog G. Periodontal conditions of adult regular dental care attendants. A 12-year longitudinal study. J Clin Periodontol 1993; 13: 714 – 22.
13. Papapanou PN, Wennström JL, Gröndahl K. A 10-year retrospective study of periodontal disease progression. J Clin Periodontol 1989; 16: 403 – 11.
14. Lindhe J, Okamoto H, Yoneyama T, Haffajee A, Socransky SS. Longitudinal changes in periodontal disease in untreated subjects. J Clin Periodontol 1989; 16: 662 – 70.
15. Axelsson P, Lindhe J, Nyström B. On the prevention of caries and periodontal disease. Results of a 15-year longitudinal study in adults. J Clin Periodontol 1991; 18: 182 – 9.
16. Lang NP, Joss A, Orsanic T, Gusberti FA, Siegrist BE. Bleeding on probing. A predictor for the progression of periodontal disease? J Clin Periodontol 1986; 13: 590 – 6.
17. Pocock SJ. Clinical trials. A practical approach. Chichester, England: John Wiley; 1986.
18. Rökning och ohälsa i munnen. En evidensbaserad kunskapssammanställning. Rapport nr 157, SBU 2002.
19. Ramberg P, Rosling B, Serino G, Hellström M-K, Socransky SS, Lindhe J. The long-term effect of systemic tetracycline used as an adjunct to non-surgical treatment of advanced periodontitis. J Clin Periodontol 2001; 28: 446 – 52.
20. Frandsen A. Mechanical oral hygiene practices. In: Löe H, Kleinman DV, editors. Dental plaque control measures and oral hygiene practices. Oxford-Washington D.C.: IRL Press Ltd.; 1986. p. 93 – 116.
21. Van der Weiden GA, Timmerman MF, Danser MM, van der Velden U. In: Lang NP, Attström R, Löe H, editors. Proceedings of the European Workshop on Mechanical Plaque Control. London: Quintessence; 1998. p. 138 – 55.
22. Heanue M, Deacon SA, Deery C, Robinson PG, Walmsley AD, Worthington HV, et al. Manual versus powered toothbrushing for oral health (Cochrane Review). In: The Cochrane Library, Issue 3. Oxford: Update Software; 2003.
23. Cronin M, Dembling W, Warren PR, King DW. A 3-month clinical investigation comparing the safety and efficacy of a novel electric toothbrush (Braun Oral-B 3D Plaque Remover) with a manual toothbrush. Am J Dent 1998; 11: 17 – 21.
24. Listgarten MA, Lindhe J, Hellden L. Effect of tetracycline and/ or scaling on human periodontal disease. J Clin Periodontol 1978; 5: 246 – 71.
25. Lindhe J, Liljenberg B, Adielsson B. Effect of long-term tetracycline therapy on human periodontal disease. J Clin Periodontol 1983; 10: 590 – 601.
26. Herrera D, Sanz M, Jepsen SJ, Needleman IG, Roldán S. A systemic review of the effect of systemic antimicrobials as an adjunct to scaling and root planing in periodontitis patients. J Clin Periodontol 2002; 29 (Suppl 3): 136 – 9.
27. Stoltze K. Elimination of Elyzol® 25 % Dentalgel matrix from periodontal pockets. J Clin Periodontol 1995; 22: 185 – 7.
28. Griffiths GS, Smart GJ, Bulman JS, Weiss G, Schrowder J, Newman HN. Comparison of clinical outcomes following treatment of chronic adult periodontitis with subgingival scaling or subgingival scaling plus metronidazole gel. J Clin Periodontol 2000; 27: 910 – 7.
29. Wennström JL, Newman HN, Macneill SR, Killoy WJ, Griffiths GS, Gillam DG, et al. Utilisation of locally delivered doxycycline in non-surgical treatment of chronic periodontitis. A comparative multi-center trial in 2 treatment approaches. J Clin Periodontol 2001; 28: 753 – 61.
30. Soskolne WA, Heasman PA, Stabholz A, Smart GJ, Palmer M, Flashner N, Newman HN. Sustained local delivery of chlorhexidine in the treatment of periodontitis. A multi-center study. J Periodontol 1997; 68: 32 – 8.
31. Killoy WJ. The use of locally-delivered chlorhexidine in the treatment of periodontitis. Clinical results. J Clin Periodontol 1998; 25: 953 – 8.
32. Salvi GE, Mombelli A, Mayfield L, Rutar A, Suvan J, Garrett S, et al. Local antimicrobial therapy after initial periodontal treatment. A randomized clinical trial comparing three biodegradable sustained release polymers. J Clin Periodontol 2002; 29: 540 – 50.
33. Pavia M, Nobile CG, Angelillo IF. Meta-analysis of local tetracycline in treating chronic periodontitis. J Periodontol 2003; 74: 916 – 32.
34. Pontoriero R, Wennström J, Lindhe J. The use of barrier membranes and enamel matrix proteins in the treatment of angular bone defects. J Clin Periodontol 1999; 26: 833 – 40.
35. Jepsen S, Eberhard J, Herrera D, Needleman I. A systematic review of guided tissue regeneration for periodontal furcation defects. What is the effect of guided tissue regeneration compared with surgical debridement in the treatment of furcation defects? J Clin Periodontol 2002; 29 (Suppl 3): 103 – 16.
36. Trombelli L, Heitz-Mayfield, LJA, Needleman I, Moles D, Scabbia A. A systematic review of graft materials and biological agents for periodontal intraosseous defects. J Clin Periodontol 2002; 29 (Suppl 3): 117 – 35.
Søkeord for nettversjon: www.tannlegetidende.no: Behandling; Gingivitt; Periodontitt, marginal.
Korrespondens: Per Ramberg, Avd. för parodontologi, Odontologiska fakulteten, Sahlgrenska akademin vid Göteborgs universitet, Box 450, SE-405 30 Göteborg, Sverige. E-post: Per.Ramberg@odontologi.gu.se